Mehanizam djelovanja neurotoksina. Otrovne i vrlo otrovne tvari s neurotoksičnim djelovanjem
Neurotoksini su tvari koje inhibiraju funkciju neurona. Neuroni su prisutni u mozgu i živčanom sustavu. Funkcije ovih jedinstvenih stanica ključne su za razne zadatke, od radnji autonomnog živčanog sustava kao što je gutanje do radnji više razine koje izvodi mozak. Neurotoksini mogu djelovati na različite načine i stoga povezane opasnosti variraju ovisno o vrsti neurotoksina i njegovoj dozi.
U nekim slučajevima neurotoksini jednostavno ozbiljno oštećuju neurone tako da ne mogu funkcionirati.
U drugim slučajevima napadaju signalne sposobnosti neurona, blokirajući otpuštanje raznih kemikalija ili ometajući proces primanja odaslanih poruka, a ponekad uzrokujući neurone da šalju lažne signale. Neurotoksini također mogu potpuno uništiti neurone.
Proizvodnja neurotoksina
Zapravo, tijelo samo proizvodi određene neurotoksine. Na primjer, velike količine mnogih neurotransmitera koji se proizvode za slanje poruka kroz živčani sustav mogu uzrokovati štetu tijelu. U nekim slučajevima tijelo proizvodi neurotoksine kao odgovor na prijetnju imunološkom sustavu. U prirodnom okolišu prisutni su i brojni neurotoksini; proizvode ih otrovne životinje; Teški metali poput olova također su neurotoksini. Ponekad se neurotoksini koriste od strane vlasti nekih zemalja za suzbijanje nereda i vođenje rata. Neurotoksini koji se koriste u takve svrhe obično se nazivaju živčanim agensima.
Izloženost neurotoksinima
Izloženost neurotoksinima može uzrokovati vrtoglavicu, mučninu, gubitak motoričke kontrole, paralizu, zamagljen vid, napadaje i moždani udar. U teškim slučajevima, učinci trovanja mogu uključivati komu i eventualnu smrt zbog prekida živčanog sustava. Konkretno, tijelo se počinje ubrzano raspadati kada neurotoksini potiskuju funkciju autonomnog živčanog sustava, budući da se niz važnih zadataka prestaje obavljati.
Trovanje
Kod akutnog trovanja, žrtva je iznenada izložena specifičnoj dozi neurotoksina. Primjer akutnog trovanja je ugriz zmije. Kronično trovanje uključuje sporo izlaganje neurotoksinu tijekom određenog vremenskog razdoblja. Primjer kroničnog trovanja je trovanje teškim metalima, kod kojeg žrtva nesvjesno prima male količine neurotoksina svaki dan.
Problem s teškim metalima je taj što se oni nakupljaju u tijelu, a ne uklanjaju iz njega, pa se u nekom trenutku oboljela osoba razboli.
Brojne tehnike mogu se koristiti za liječenje trovanja neurotoksinima. Mnogi od njih oslanjaju se na pomoćnu njegu kako bi omogućili obavljanje zadataka s kojima se tijelo ne može nositi dok se stanje pacijenta ne stabilizira. Ako se to dogodi, pacijent se može oporaviti, ali će se kasnije često morati suočiti s nuspojavama povezanima s otrovom. U nekim slučajevima, kemikalije se koriste za blokiranje rada neurotoksina ili njihovo ispiranje iz tijela. U drugim slučajevima možda neće biti lijeka za trovanje, a cilj liječenja je osigurati udobnost pacijenta.
Izvor: wisegeek.com
Foto: newearth.media

Rak gušterače vrlo je čest. Liječenje raka gušterače određuje se ovisno o mjestu i stadiju raka. Mogućnost liječenja odabire se na temelju dobi i općeg zdravlja pacijenta. Liječenje raka ima za cilj ukloniti rak kada je to moguće ili spriječiti daljnji rast tumora. Ako se rak gušterače dijagnosticira u uznapredovalom stadiju i bilo koja mogućnost liječenja...

Parkinsonova bolest može pogoditi bilo koga. Osobe koje boluju od Parkinsonove bolesti zahtijevaju puno brige i pažnje. Za pacijenta postaje vrlo frustrirajuće kada ne može razumjeti druge ili se brinuti za sebe. Za to vrijeme pružite podršku pacijentu. Nemojte se ljutiti niti iritirati pacijenta kada vas ne razumije. Govorite jasno, pozitivno i komunicirajte s pacijentom. Kontakt očima je bitan...

Vestibularni sustav može patiti od određenih poremećaja koji variraju od labirintitisa do benigne paroksizmalne položajne vrtoglavice, što ne samo da može utjecati na slušne sposobnosti osobe, već može dovesti i do niza drugih zdravstvenih problema. Uho ne samo da čuje, već pomaže iu održavanju ravnoteže u svakodnevnim aktivnostima. Postoje određene tekućine u našim ušima koje...
Leonid Zavalski
Neurotoksini se sve više koriste u medicini u terapeutske svrhe.
Neki neurotoksini različite molekularne strukture imaju sličan mehanizam djelovanja, uzrokujući fazne prijelaze u membranama živčanih i mišićnih stanica. Važnu ulogu u djelovanju neurotoksina ima hidratacija, koja značajno utječe na konformaciju otrova i receptora koji međusobno djeluju.
Podaci o otrovnosti napuhača (maki-maki, pas, napuhač i dr.) sežu još u antičko doba (više od 2500 godina pr. Kr.). Od Europljana, prvi je dao detaljan opis simptoma trovanja slavni moreplovac Cook, koji se zajedno sa 16 mornara počastio ribom puferom tijekom svog drugog putovanja oko svijeta 1774. godine. Imao je sreće, jer je “jedva dotakao filet”, dok je “svinja, koja je jela iznutrice, crknula i crknula”. Začudo, Japanci si ne mogu uskratiti užitak kušanja ove, s njihove točke gledišta, delicije, iako znaju koliko je pažljivo treba pripremiti i koliko je opasno jesti.
Prvi znakovi trovanja pojavljuju se unutar nekoliko minuta do 3 sata nakon konzumacije fugu. Nesretni jedač najprije osjeti trnce i obamrlost jezika i usana, a zatim se proširi na cijelo tijelo. Tada počinju glavobolja i bolovi u trbuhu, a ruke mi se paraliziraju. Hod postaje nesiguran, javlja se povraćanje, ataksija, stupor i afazija. Disanje postaje otežano, snižava se krvni tlak, pada tjelesna temperatura, razvija se cijanoza sluznica i kože. Bolesnik pada u komatozno stanje, a ubrzo nakon prestanka disanja prestaje i srčana aktivnost. Jednom riječju, tipična slika djelovanja živčanog otrova.
Godine 1909. japanski istraživač Tahara izolirao je aktivni sastojak iz fugua i nazvao ga tetrodotoksin. Međutim, tek 40 godina kasnije bilo je moguće izolirati tetrodotoksin u kristalnom obliku i utvrditi njegovu kemijsku formulu. Za dobivanje 10 g tetrodotoksina japanski znanstvenik Tsuda (1967.) morao je obraditi 1 tonu jajnika fugua. Tetrodotoksin je spoj aminoperhidrokinazolina s gvanidinskom skupinom i ima izrazito visoku biološku aktivnost. Kako se pokazalo, prisutnost gvanidinske skupine igra odlučujuću ulogu u pojavi toksičnosti.
Istodobno s proučavanjem otrova riba zubaca i napuhača, mnogi laboratoriji diljem svijeta proučavali su toksine izolirane iz tkiva drugih životinja: daždevnjaka, tritona, otrovnih žaba krastača i drugih. Pokazalo se zanimljivim da su u nekim slučajevima tkiva potpuno različitih životinja koje nisu genetski srodne, posebice kalifornijski triton Taricha torosa, ribe iz roda Gobiodon, srednjoameričke žabe Atelopus, australske hobotnice Hapalochlaena maculosa, proizvele isti otrov tetrodotoksin.
Djelovanje tetrodotoksina vrlo je slično drugom neproteinskom neurotoksinu, saksitoksinu, kojeg proizvode jednostanični flagelirani dinoflagelati. Otrov ovih jednostaničnih organizama s bičem može se koncentrirati u tkivima mekušaca dagnji tijekom masovne reprodukcije, nakon čega dagnje postaju otrovne kada ih konzumiraju ljudi. Istraživanje molekularne strukture saksitoksina pokazalo je da njegove molekule, poput tetrodotoksina, sadrže gvanidinsku skupinu, čak dvije takve skupine po molekuli. Inače, saksitoksin nema zajedničkih strukturnih elemenata s tetrodotoksinom. Ali mehanizam djelovanja ovih otrova je isti.
Patološki učinak tetrodotoksina temelji se na njegovoj sposobnosti da blokira provođenje živčanih impulsa u ekscitabilnim živčanim i mišićnim tkivima. Jedinstvenost djelovanja otrova leži u činjenici da u vrlo niskim koncentracijama - 1 gama (stotisućiti dio grama) po kilogramu živog tijela - blokira ulaznu struju natrija tijekom akcijskog potencijala, što dovodi do smrti. . Otrov djeluje samo na vanjskoj strani membrane aksona. Na temelju tih podataka japanski znanstvenici Kao i Nishiyama pretpostavili su da tetrodotoksin, čija je veličina gvanidinske skupine bliska promjeru hidratiziranog natrijeva iona, ulazi u usta natrijeva kanala i zaglavi u njemu te se stabilizira na izvana ostatkom molekule, čije dimenzije premašuju promjer kanala. Slični podaci dobiveni su proučavanjem blokirajućeg učinka saksitoksina. Razmotrimo fenomen detaljnije.
U mirovanju se između unutarnje i vanjske strane membrane aksona održava razlika potencijala od približno 60 mV (vanjski potencijal je pozitivan). Kada se živac pobudi na mjestu primjene u kratkom vremenu (oko 1 ms), razlika potencijala mijenja predznak i doseže 50 mV - prva faza akcijskog potencijala. Nakon postizanja maksimuma potencijal se u danoj točki vraća u početno stanje polarizacije, ali njegova apsolutna vrijednost postaje nešto veća nego u mirovanju (70 mV) – druga faza akcijskog potencijala. Unutar 3-4 ms, akcijski potencijal u ovoj točki na aksonu vraća se u stanje mirovanja. Impuls kratkog spoja dovoljan je da pobudi susjedni dio živca i repolarizira ga u trenutku kada se prethodni dio vrati u ravnotežu. Dakle, akcijski potencijal se širi duž živca u obliku neprigušenog vala koji putuje brzinom od 20-100 m/s.
Hodgkin i Huxley sa svojim suradnicima detaljno su proučavali proces širenja živčanih podražaja i pokazali da je u stanju mirovanja membrana aksona nepropusna za natrij, dok kalij slobodno difundira kroz membranu. Kalij koji "istječe" odnosi pozitivan naboj, a unutarnji prostor aksona postaje negativno nabijen, sprječavajući daljnje otpuštanje kalija. Kao rezultat toga, ispada da je koncentracija kalija izvan živčane stanice 30 puta manja nego unutra. S natrijem je situacija suprotna - u aksoplazmi je njegova koncentracija 10 puta niža nego u međustaničnom prostoru.
Molekule tetrodotoksina i saksitoksina blokiraju natrijev kanal i, kao rezultat, sprječavaju prolaz akcijskog potencijala kroz akson. Kao što se vidi, uz specifičnu interakciju gvanidinske skupine s ušćem kanala (interakcija tipa “ključ-brava”), određenu funkciju u interakciji ima i preostali dio molekule, predmet do hidratacije molekulama vode iz vodeno-slane otopine okružene membranom.
Važnost istraživanja djelovanja neurotoksina teško se može precijeniti, jer su nam po prvi put omogućila da se približimo razumijevanju tako temeljnih fenomena kao što je selektivna ionska propusnost staničnih membrana, koja je u osnovi regulacije vitalnih funkcija tijela . Korištenjem visoko specifičnog vezanja tetrodotoksina obilježenog tricijem, bilo je moguće izračunati gustoću natrijevih kanala u aksonskoj membrani različitih životinja. Tako je u divovskom aksonu lignje gustoća kanala bila 550 po kvadratnom mikrometru, au žabljem sartorius mišiću 380.
Specifično blokiranje vodljivosti živaca omogućilo je korištenje tetrodotoksina kao snažnog lokalnog anestetika. Trenutno su mnoge zemlje već uspostavile proizvodnju lijekova protiv bolova na temelju tetrodotoksina. Postoje dokazi o pozitivnom terapijskom učinku neurotoksinskih lijekova kod bronhijalne astme i konvulzivnih stanja.
Mehanizmi djelovanja morfina sada su vrlo detaljno proučeni. Medicina i farmakologija odavno poznaju svojstva opijuma za ublažavanje bolova. Već 1803. godine njemački farmakolog Fritz Serthuner uspio je opijumsku drogu pročistiti i iz nje izdvojiti djelatnu tvar - morfij. Lijek morfij bio je široko korišten u kliničkoj praksi, osobito tijekom Prvog svjetskog rata. Njegov glavni nedostatak je nuspojava, koja se izražava u stvaranju kemijske ovisnosti i ovisnosti tijela o lijeku. Stoga se pokušalo pronaći zamjenu za morfij s jednako učinkovitim lijekom protiv bolova, ali bez nuspojava. Međutim, sve nove tvari, kako se pokazalo, također uzrokuju sindrom ovisnosti. Takva je sudbina zadesila heroin (1890.), meperidin (1940.) i druge derivate morfija. Mnoštvo molekula opijata različitih oblika pruža osnovu za točno utvrđivanje strukture opijatnog receptora na koji je vezana molekula morfija, slično receptoru tetrodotoksina.
Sve molekule analgetski aktivnih opijata imaju zajedničke elemente. Molekula opijuma ima kruti T-oblik, predstavljen s dva međusobno okomita elementa. U bazi T-molekule nalazi se hidroksilna skupina, a na jednom kraju vodoravne trake nalazi se atom dušika. Ovi elementi čine "osnovnu osnovu" ključa koji otvara receptorsku bravu. Čini se značajnim da samo lijevorotirajući izomeri serije morfina imaju analgetsko i euforično djelovanje, dok su desnorotirajući izomeri lišeni takvog djelovanja.
Brojna istraživanja su utvrdila da receptori za opijate postoje u tijelima svih kralježnjaka bez iznimke, od morskih pasa do primata, uključujući i čovjeka. Štoviše, pokazalo se da je samo tijelo sposobno sintetizirati supstance slične opijumu zvane enkefalini (metionin-enkefalin i leucin-enkefalin), koje se sastoje od pet aminokiselina i nužno sadrže određeni morfijski "ključ". Enkefaline oslobađaju posebni enkefalinski neuroni i uzrokuju opuštanje tijela. Kao odgovor na vezivanje enkefalina za opijatni receptor, kontrolni neuron šalje signal opuštanja glatkim mišićima i percipira ga najstarija tvorevina živčanog sustava – limbički mozak – kao stanje vrhunskog blaženstva, odnosno euforije. To se stanje, primjerice, može dogoditi nakon stresa, dobro obavljenog posla ili dubokog seksualnog zadovoljstva, što zahtijeva određenu mobilizaciju tjelesnih snaga. Morfin pobuđuje opijatni receptor, poput enkefalina, čak i kada nema razloga za blaženstvo, na primjer, u slučaju bolesti. Dokazano je da stanje nirvane jogija nije ništa više od euforije koja se postiže otpuštanjem enkefalina kroz autotrening i meditaciju. Na taj način jogiji otvaraju pristup glatkim mišićima i mogu regulirati rad unutarnjih organa, čak i zaustaviti otkucaje srca.
Što su neurotoksini? To su tvari koje ometaju električnu aktivnost živaca, onemogućujući im pravilan rad.
Kako neurotoksini uništavaju živčane stanice?
Neurotoksini su tvari koje stupaju u interakciju sa živčanim stanicama, pretjerano ih stimuliraju ili prekidaju komunikaciju među njima. To su štetni procesi za živčane stanice koji utječu na njihove kemijske procese. Istraživanja jasno pokazuju da neurotoksini smanjuju život živčanih stanica. Ti su toksini povezani s raznim poremećajima mozga i neurodegenerativnim bolestima poput Alzheimerove bolesti, Huntingtonove koreje i Parkinsonove bolesti.
Neurotoksini su značajno proliferirali tijekom posljednjih nekoliko desetljeća. Mnogi od njih se koriste u hrani koju jedemo i vodi koju pijemo. Najviše se koriste neurotoksini u brzoj hrani, konzerviranoj hrani, a često se koriste i u formulama za dojenčad.
Neurotoksini u hrani
Ako imate dijete ili malu djecu, trebali biste obratiti posebnu pozornost na 10 najčešćih neurotoksina navedenih u nastavku. Djeca su najosjetljivija na neurotoksine jer su njihova tijela još u razvoju. Prerađena hrana poput čipsa, slatkiša i čokolade često sadrži neurotoksine. Ako naiđete na hranu koja sadrži bilo koji od dolje navedenih neurotoksina, trebali biste je izbjegavati jesti.
Aspartam (aka Equal, AminoSweet, NutraSweet, Spoonful) - Najčešće se koristi u hrani bez šećera. Posebno u žvakaćim gumama i pićima bez šećera. Većina aspartama dobiva se iz otpada genetski modificiranih bakterija. Istraživanja pokazuju da aspartam može uzrokovati dijabetes, migrene, zatajenje bubrega, napadaje, sljepoću, pretilost, neurološke poremećaje, mentalne bolesti i tumore mozga.
Mononatrijev glutamat (poznat i kao MSG) najčešće se koristi u čipsu, konzerviranoj hrani, dječjoj hrani i brojnoj nezdravoj hrani. Neovisni istraživači vjeruju da MSG igra važnu ulogu u razvoju neurodegenerativnih bolesti mozga, uključujući Alzheimerovu, Parkinsonovu i Huntingtonovu bolest. Dokazi koji podupiru ovu tvrdnju dolaze iz činjenice da mononezasićeni grutani oštećuju neurone, posebice moždane stanice.
Sukraloza (također poznata kao Splenda) je umjetni zaslađivač koji se koristi u proizvodima bez šećera, posebno u pićima. Sukraloza je otkrivena sasvim slučajno dok su se provodila istraživanja za stvaranje novog insekticida. Stoga mnogi znanstvenici smatraju da sukralozu treba smatrati insekticidom. Ovaj toksin mnogi identificiraju kao kemijskog rođaka DDT-a. Sukraloza je klorirani spoj, a razgradnja ove vrste spoja u tijelu oslobađa otrovne kemikalije.
Aluminij – Ovaj metal je čest u vodi za piće i cjepivima. Tijelo dobro apsorbira aluminij. Limunska kiselina ili citrat mogu značajno povećati njegovu apsorpciju. Cjepiva su jedan od glavnih uzroka trovanja aluminijem jer se aluminij ubrizgava izravno u tijelo.
Živa - ovaj teški metal čest je u ribljim proizvodima i cjepivima. Živa se može naći i u vodi za piće. Jedan je od najotrovnijih neurotoksina jer lako uništava moždano tkivo.
Fluorid (natrijev fluorid). Ovaj je toksin vrlo čest u pitkoj vodi i običnim pastama za zube. U prošlosti se fluorid koristio kao otrov za štakore. Fluorid koji se koristi u potrošačkim proizvodima mješavina je vrlo opasnih kemikalija. Također poznat kao natrijev fluorid, ne miješa se s prirodnim kalcijevim fluoridom. Iz tog razloga paste za zube s fluorom imaju oznake upozorenja.
Hidrolizirani biljni protein – Ovaj nezdravi sastojak hrane čest je u većini nezdravih namirnica. Sadrži visoke koncentracije glutamata i aspartata koji mogu stimulirati živčane stanice i u konačnici dovesti do njihove smrti.
Kalcijev kazeinat – Ovaj se toksin obično koristi u proteinskim dodacima, nezdravoj hrani i čokoladnim energetskim pićima. Oštećuje mozak zbog svojih neurotoksičnih svojstava.
Natrijev kazeinat – Ova vrsta proteina česta je u mliječnim proizvodima i nezdravoj hrani. Vjeruje se da uzrokuje probleme s autizmom i gastrointestinalnim bolestima.
Ekstrakt kvasca je popularan sastojak hrane u mnogim procesiranim namirnicama kao što je konzervirana hrana. Toksičan je za mozak.
u biokemiji
Mehanizam djelovanja neurotoksina zmijskog otrova
Uvod
kemija zmijski otrov
Zmijski otrovi jedinstvena su skupina biološki aktivnih spojeva po svom kemijskom sastavu i fiziološkom djelovanju. Njihova toksična i ljekovita svojstva poznata su čovječanstvu od davnina. Dugo je vrijeme zanimanje za proučavanje ovih otrovnih proizvoda bilo ograničeno na potrebe medicinske prakse. Najveći dio rada posvećen je opisu kliničke slike trovanja, pronalaženju metoda specifične i nespecifične terapije, kao i korištenju zmijskih otrova i njihovih pripravaka kao terapeutskih sredstava. Racionalna uporaba zmijskih otrova u medicini nemoguća je bez eksperimentalnog proučavanja i teorijskog opravdanja suštine reakcija koje se razvijaju u tijelu kao odgovor na uvođenje određenog otrova. Proučavanje pojedinih mehanizama djelovanja zmijskog otrova na organizam nužno je za stvaranje znanstveno utemeljenih metoda liječenja.
Nedovoljno poznavanje mehanizama toksičnog djelovanja zmijskog otrova često ne dopušta liječnicima da brzo i učinkovito olakšaju stanje žrtve. U nekim slučajevima uzima se u obzir samo vanjska slika trovanja, a klinička skrb je ograničena na simptomatska sredstva bez uzimanja u obzir specifičnih učinaka otrova na vitalne sustave tijela.
Treba napomenuti da zmijski otrovi imaju jak toksični učinak samo u letalnim i subletalnim dozama. Male doze ne izazivaju nikakve kliničke manifestacije trovanja i dugo se koriste u praktičnoj medicini. Međutim, terapijska primjena često se provodi empirijski bez dovoljnog teorijskog opravdanja, što za sobom povlači pogreške. Nema potrebe dokazivati da se učinkovita uporaba zmijskih otrova u klinici treba temeljiti na dubokom poznavanju njihovog sastava i svojstava, a prije svega na eksperimentalnim istraživanjima koja bi trebala otkriti fiziološku prirodu i mehanizme djelovanja ovih otrovnih tvari. i pomoći liječnicima da znanstveno koriste otrove u terapeutske svrhe. U istraživačkim laboratorijima došlo je do naglog porasta interesa za zootoksine, a posebno za zmijske otrove, u vezi s dobivanjem iz njih u čistom obliku niza komponenti koje imaju vrlo specifične učinke i određene biološke strukture.
Svrha ovog rada je osvijetliti trenutno stanje eksperimentalnog proučavanja zmijskih otrova, otkriti mehanizme patofizioloških učinaka na najvažnije funkcionalne sustave organizma.
Stanje kemije zmijskih otrova.
Priprava otrova i njegova fizikalno-kemijska svojstva.
Najjednostavniji način dobivanja otrovnih izlučevina zmija je mehanička masaža otrovnih žlijezda. Danas se umjesto mehaničke masaže često koristi stimulacija električnom strujom.
Električna stimulacija nije samo nježnija metoda skupljanja otrova, već vam također omogućuje da dobijete veću količinu otrova. Količina otrova dobivena od jedne jedinke ovisi o veličini tijela zmije, njenom fiziološkom stanju, broju ponovljenih doza otrova, kao io nizu uvjeta okoline. Treba napomenuti da držanje zmija u zatočeništvu ne utječe samo na količinu dobivenog otrova, već i na njegovu toksičnost. Tako se u otrovu kobre opaža smanjenje toksičnosti nakon šest mjeseci zatočeništva. Otrov poskoka mijenja svoju otrovnost tek nakon 2 godine držanja u rasadniku. Što se tiče malih zmija (poskok, bakrenjak, eph), njihovo držanje u serpentarijima tijekom cijele godine ne utječe na svojstva otrova. Svježe ekstrahiran zmijski otrov je blago opalescentna, viskozna, prilično prozirna tekućina; boja otrova varira od svijetložute do limunaste.
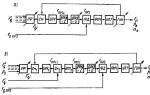
Aktivna reakcija otrova obično je kisela. Njihove vodene otopine su nestabilne i nakon nekoliko dana gube toksičnost. Postaju mnogo otporniji na čimbenike okoliša nakon sušenja iznad kalcijevog klorida ili liofilizacije. Otrovi su prilično termostabilni i mogu podnijeti zagrijavanje do 120 stupnjeva Celzijusa u kiseloj sredini bez gubitka aktivnosti. Kemijski reagensi razorno djeluju na otrove: KMnO 4, eter, kloroform, etanol metilensko modrilo. Utječu i fizički čimbenici: UV zračenje, x-zrake. Kemijska analiza pokazuje prisutnost i organskih i anorganskih tvari u zmijskim otrovima. Prema modernim konceptima, toksična aktivnost i biološka svojstva zmijskog otrova povezana su s njihovim proteinskim komponentama. Glavne faze proučavanja kemijskog sastava i strukture toksičnih polipeptida zmijskog otrova. Pitanja o kemijskoj prirodi i mehanizmima djelovanja zmijskih otrova privukla su pozornost istraživača. U ranim studijama, toksični učinak bio je povezan s aktivnošću enzima prisutnih u otrovima. Trenutno je općeprihvaćeno gledište da su glavna toksična svojstva određena neenzimskim polipeptidima, uz koje otrovi sadrže moćne enzimske sustave, čija priroda i specifičnost djelovanja u većini slučajeva određuje jedinstvenost cjelovite slike od trovanja. Postignuća i uspjesi u području proučavanja kemijskog sastava otrova usko su povezani s razvojem i usavršavanjem metoda frakcioniranja i pročišćavanja složenih smjesa spojeva visoke molekulske mase. Do 1960-ih proučavanje otrova uglavnom je koristilo dijalizu kroz polupropusne membrane i elektroforetsko odvajanje. Razvoj metoda gel filtracije, kromatografije ionske izmjene, ultracentrifugiranja, kao i razvoj i automatizacija metoda za analizu primarne strukture makromolekula omogućio je dešifriranje slijeda aminokiselinskih ostataka toksičnih polipeptida većine zmija u relativno kratkom vremenu. kratko vrijeme. 1.Terminologija i klasifikacija toksičnih polipeptida kemija zmijski otrov Donedavno su postojale terminološke poteškoće pri pokušaju komparativne analize funkcionalnih i strukturnih značajki različitih neenzimskih toksičnih polipeptida zmijskih otrova. To se uglavnom odnosi na polipeptide izolirane iz otrova zmija iz obitelji Elapidae. U prvim fazama proučavanja kemijskog sastava otrova takve su poteškoće bile neizbježne i objašnjavale su se nedovoljnim stupnjem pročišćavanja pojedinih polipeptida, što je u većini slučajeva otežavalo određivanje specifične prirode njihovog djelovanja. Zbog toga su različiti autori davali različite nazive polipeptidima za koje se pokazalo da su vrlo bliski, a ponekad i identični, po svojoj kemijskoj strukturi i farmakološkom djelovanju. Posebno je skupina kardiotoksina označena kao faktor koji depolarizira skeletne mišiće; toksin Y; izravni litički faktor - PLF; kobramini A i B; citotoksini 1 i 2. Neki su se autori pri izboru naziva bazirali na patofiziološkim učincima (kardiotoksin, PLP, citotoksin), drugi su isticali neka kemijska svojstva polipeptida, primjerice njegovu bazičnost (kobramin), dok su treći davali brojčanu ili slovnu oznaku polipeptida. frakcija. Tek posljednjih godina ustanovljena je velika sličnost u kemijskoj strukturi ovih polipeptida. Dobiveni su dokazi da su hemolitička, citotoksična, kardiotoksična i druge vrste aktivnosti svojstvene većini ovih toksina. Stoga je skupina bazičnih polipeptida koji nemaju specifično neurotoksično djelovanje, ali učinkovito djeluju na biološke membrane, nazvana membranski aktivni polipeptidi (MAP). Na temelju usporedne analize primarne strukture i fiziološkog djelovanja, koja je pokazala veliku međusobnu sličnost neurotoksičnih polipeptida, oni su objedinjeni pod zajedničkim pojmom - neurotoksin. Tako su iz otrova zmija iz porodice Elapidae do sada izolirani svi toksični polipeptidi koji nemaju enzimska svojstva, a prema mehanizmu djelovanja i podijeljeni su u tri skupine. U prvu skupinu spadaju polipeptidi koji selektivno i specifično blokiraju kolinergičke receptore subsinaptičke membrane neuromuskularnog spoja – postsinaptički neurotoksini (post-NT). Drugu skupinu predstavljaju polipeptidi koji selektivno djeluju na presinaptičke završetke mioneuralnih sinapsi i remete proces otpuštanja acetilkolina - presinaptički neurotoksini (pre-NT). Treća skupina uključuje polipeptide koji aktivno utječu na membranske strukture stanica, uključujući ekscitabilne, uzrokujući njihovu depolarizaciju - membranski aktivni polipeptidi (MAP). 2. Kemija postsinaptičkih neurotoksina Unatoč činjenici da su post-NT izolirani iz otrova kobre slični po svojim farmakološkim svojstvima, s gledišta kemijske strukture mogu se podijeliti u dvije vrste. Tip 1 uključuje post-HT, koji je jednostavan polipeptidni lanac koji se sastoji od 60-62 aminokiselinskih ostataka koji imaju 4 disulfidna mosta (Slika 1. A) i ima osnovna svojstva, molekulsku težinu od oko 7000 (post-HT-1) . Tip 2 uključuje post-NT, koji se sastoji od 71-74 aminokiselinskih ostataka, ima 5 disulfidnih mostova (slika 1, B), molekularne težine od oko 8000 (post-NT-2). Slika 1. Primarna struktura neurotoksina II (A) i neurotoksina I (B) iz otrova srednjoazijske kobre Post - NT-1 izgrađeni su od 15 uobičajenih aminokiselinskih ostataka, a u njihovom sastavu u pravilu nema Ala, Met i Phen. Naprotiv, javlja se post-HT-2 alanin. Zanimljiva značajka otrova srednjoazijske kobre je prisutnost obje vrste neurotoksina u njemu. Štoviše, u neurotoksinu koji sadrži 73 aminokiselinska ostatka, Arg ili Lys 51, karakteristični za sve post-HT-2, zamijenjeni su s Glu. Zasićenost post-HT 1 i 2 disulfidnih veza ukazuje na njihovu važnu funkcionalnu važnost u održavanju biološki aktivne konformacije molekule. Redukcija disulfidnih veza dovodi do gubitka 92% aktivnosti post-NT-1 i 50% post-NT-2. ponovna oksidacija vraća izvornu aktivnost neurotoksina. Očito je veća otpornost post-NT-2 na kemijske utjecaje posljedica prisutnosti pete disulfidne veze, koja stabilizira dio polipeptidnog lanca. U isto vrijeme, u post-NT-1 taj isti dio molekule je najizduženiji i nema disulfidne mostove. Prisutnost mostova određuje otpornost post-LT-a na toplinske učinke. Stoga, u kiselom okruženju, post-NT može izdržati zagrijavanje do 100°C tijekom 30 minuta bez primjetnog gubitka aktivnosti ili tretmana s 8M ureom tijekom 24 sata, ali se inaktivira alkalijama. Dešifriranje primarne strukture neurotoksičnih polipeptida omogućilo je postavljanje pitanja o lokalizaciji i strukturi aktivnog središta molekule koja je u interakciji s kolinskim receptorom. Proučavanje strukture ovih polipeptida ukazuje na prisutnost i α i β struktura u molekulama neurotoksina. Središnji dio post-HT-1 molekule, bez disulfidnih veza, može imati veću α-spiralnost. Osim toga, hidrofilna priroda većine bočnih lanaca aminokiselinskih ostataka koji čine niz od položaja 24-25 do položaja 39-40 može uzrokovati projekciju ove petlje na vanjsku stranu molekule, tako da je moguće da je aktivno središte lokalizirano u ovoj regiji. Važna je analiza položaja i kemijske modifikacije nepromjenjivih aminokiselina pronađenih u homolognim neurotoksinima u istim regijama. Ove aminokiseline, sačuvane tijekom evolucije u identičnim dijelovima polipeptidnog lanca, mogu sudjelovati u organizaciji aktivnog centra ili osigurati održavanje aktivne konformacije molekule. Prisutnost konstantnih aminokiselina zahtijeva prisutnost invarijantnog tripletnog genskog koda u molekuli DNA potrebnog za sintezu danog slijeda aminokiselina. Budući da je meta za post-HT, kao i za acetilkolin, kolinergički receptor, očito aktivna mjesta neurotoksina trebala bi biti slična kvaternim amonijevim i karbonilnim skupinama acetilkolina. Utvrđeno je da slobodne amino skupine, uključujući N-terminalne, nisu obvezne osigurati toksičnu aktivnost. Acitilacija 6 amino skupina u neurotoksinu iz otrova tajlandske kobre dovela je do gubitka 1/3 aktivnosti. Moglo bi se pretpostaviti da karbonilne skupine peptidnog sastava, uvijek prisutne u post-HT molekuli, mogu biti važne u osiguravanju toksičnosti. Međutim, oni su nedostupni u reakciji interakcije s receptorom. U većoj mjeri, bočne skupine bočnih lanaca nepromjenjive asparaginske kiseline i asparagina ispunjavaju ovaj zahtjev. Modifikacija asparaginske kiseline glicin metil esterom dovodi do gubitka aktivnosti od 75% izvorne vrijednosti. Ireverzibilno vezanje između post-NT i kolinergičkog receptora ne može se objasniti samo interakcijom gvanidinskih i karbonilnih skupina post-NT s odgovarajućim regijama receptora. Njihova bi interakcija trebala biti uglavnom elektrostatske prirode, međutim, kompleks receptor-toksin ne disocira u koncentriranim slanim otopinama. Vjerojatno ove dvije funkcionalne skupine služe kao "mjesta prepoznavanja" tijekom početnog kontakta post-NT i receptora. Konačno ireverzibilno vezanje određeno je interakcijom protein-protein, koja već uključuje druga područja post-HT i kolinergičkog receptora. 3. Kemija presinaptičkih neurotoksina Druga skupina neurotoksina, presinaptički neurotoksini (pre-NT), rijetko se nalaze u zmijskim otrovima. Samo su neki od njih izolirani u pročišćenom obliku i proučavani. U obitelji Elapidae presinaptičke NT nalaze se u otrovu australskog tajpana - tipoksin, australske tigraste zmije - noteksin i u otrovu kraita - β-bungarotoksin. Krotoksin, neurotoksin iz otrova čegrtuše, ima dominantan presinaptički učinak na neuromuskularne spojeve kod vodozemaca i postsinaptički učinak kod sisavaca. Za razliku od post-HT, neurotoksini 2. skupine izgrađeni su od većeg broja aminokiselinskih ostataka i shodno tome imaju veću molekularnu masu. Osim toga, neki od njih su kompleksi koji se sastoje od podjedinica. Jedan od prvih pre-NT dobivenih korištenjem zonske elektroforeze na škrobnom gelu i naknadno pročišćen kromatografijom na KM-Sephadexu s ponovljenom rekromatografijom bio je β-bungarotoksin. β-bungarotoksin je građen od približno 179 aminokiselinskih ostataka, među kojima dominiraju asparaginska kiselina (22 ostatka), glicin (16), lizin (13), arginin (14), tirozin (13). Prisutnost 20 cistinskih ostataka ukazuje da je molekula β-bungarotoksina stabilizirana s najmanje 10 sulfidnih veza. Molekularna težina neurotoksina je 28500. Pretpostavlja se da β-bungarotoksin nema enzimska svojstva i da je homogen. Međutim, utvrđeno je da se β-bungarotoksin sastoji od dvije podjedinice molekulske mase 8800 i 12400, a proučavajući učinke β-bungarotoksina na oksidativnu fosforilaciju u mitohondrijima živčanih završetaka, došli su do zaključka da toksin ima fosfolipazu. aktivnost. Notexin je dobiven kromatografijom ionske izmjene u gradijentu amonijevog acetata. Glavna neurotoksična komponenta noteksina, koja čini 6% sirovog, nerafiniranog otrova, izolirana je ponovljenom kromatografijom u obliku pripravka koji sadrži 27% noteksina. 4. Učinak otrova na neuromuskularni prijenos Najviše je proučavan mehanizam poremećaja prijenosa ekscitacije u mioneuralnim sinapsama pod utjecajem zmijskog otrova. Već prva opažanja slike uginuća otrovane životinje, u kojoj su dominirali simptomi paralize skeletnih i respiratornih mišića, nametnula su proučavanje ovog fenomena u strogim laboratorijskim uvjetima. Brojni pokusi na izoliranim neuromuskularnim pripravcima pokazali su da zmijski otrovi blokiraju prijenos ekscitacije od živca do mišića, smanjuju ekscitabilnost na izravni i neizravni podražaj te uzrokuju depolarizaciju živčanih i mišićnih membrana. Inhibicija neuromuskularnog prijenosa pod utjecajem otrova može se ostvariti kroz dva mehanizma. Jedan od njih povezan je s blokirajućim učinkom otrova na krajnjoj ploči. Drugi se temelji na depolarizirajućem učinku na ekscitabilne membrane. Međutim, kada se koristi cjeloviti otrov, teško je razlikovati ova dva mehanizma, budući da njegov depolarizirajući učinak dovodi do blokade propagiranja ekscitacije u živčanim vlaknima, au visokim koncentracijama otrov uzrokuje kontrakture mišića. Otrov sprječava depolarizirajuće djelovanje acetilkolina na izolirane mišiće, dok spojevi acetilkolinesteraze smanjuju njegov blokirajući učinak. U eksperimentima je krotoksin blokirao kontrakciju mišića zbog neizravne stimulacije i nije imao učinka na membranski potencijal. Međutim, studije o učinku otrova dviju vrsta (sa i bez krotamina) izvijestile su o praktički nepovratnom blokirajućem učinku otrova bez krotamina na neuromuskularni prijenos kod mačaka i štakora, kako na mišićne membrane tako i na specifične receptore postsinaptičke membrane. Neuromuskularni blok pod utjecajem otrova koji je sadržavao krotamin postignut je depolarizacijom mišićnih membrana. Otrov zmije također može poremetiti neuromuskularni prijenos, uzrokujući perifernu paralizu zbog nepovratne blokade specifičnih acetilkolinskih receptora. Također inhibira električnu aktivnost mišićnih vlakana. Imunokemijska analiza pokazala je prisutnost proteinske frakcije slične postsinaptičkoj u otrovu α- toksin iz otrova crnovrate kobre. Na Institutu za bioorgansku kemiju nazvan. Akademici M.M. Šemjakina<#"justify">5. Postsinaptički neurotoksini (post-NT) Za razliku od cijelog kobrinog otrova, post-NT selektivno blokiraju prijenos ekscitacije u neuromuskularnom spoju bez utjecaja na električna svojstva živca i mišića. Inkubacija izoliranih neuromuskularnih pripravaka tijekom jednog sata u otopini koja sadrži post-NT u koncentraciji od oko 1 μg/ml dovodi do progresivnog smanjenja amplitude potencijala krajnje ploče (EPP). Inhibicijski učinak raste s povećanjem učestalosti stimulacije, dok se amplituda EPP-a smanjuje bez značajnih promjena u njihovoj učestalosti. Čak i pri visokim koncentracijama, post-NT nije imao učinak na potencijale mirovanja mišićnih i motoričkih završetaka. Membrane kolinergičkih receptora skeletnih mišića kralježnjaka najosjetljivije su na učinke post-NT. Istodobno, somatski mišići morskih mekušaca i srce lampure otporni su na djelovanje neurotoksina kobre. Specifične razlike u osjetljivosti kolinergičkih receptora kod različitih predstavnika kralješnjaka (žabe, kokoši, mačići, štakori). Pretpostavlja se da post-NT nisu izravni konkurenti acetilkolinu za aktivno mjesto kolinergičkog receptora. 6. Presinaptički neurotoksini (pre-NT) Neurotoksini s presinaptičkim djelovanjem selektivno utječu na mehanizam oslobađanja acetilkolina bez utjecaja na osjetljivost na posrednik postsinaptičkih struktura. Obrada izoliranog neuromuskularnog preparata β- bungarotoksin nakon početnog razdoblja povećanja učestalosti dovodi do potpune eliminacije PEP-a. Brzina početka inhibitornog učinka ovisi i o koncentraciji pre-NT i o učestalosti stimulacije. Također je utvrđena ovisnost vremena nastanka blokade neuromuskularnog prijenosa o temperaturi okoline. Tako je tipoksin (1 μg/ml) na temperaturi od 37 °C izazvao inhibiciju lijeka na sat vremena; kada je temperatura pala na 28 °C, vodljivost je ostala do 4 sata inkubacije. Pre-NT ne smanjuju odgovor izoliranih mišića na egzogeni acetilkolin i ne utječu na provođenje ekscitacije duž živčanih završetaka. Drugi dokazi selektivnog presinaptičkog djelovanja β- bungarotoksina dobiveni su na kulturi tkiva bez živaca dobivenoj iz mioblasta 10 dana starih pilećih embrija. Predinkubacija α- bungarotoksin potpuno je eliminirao depolarizaciju uzrokovanu naknadnim uvođenjem acetilkolina u medij. U ovim uvjetima β- bungarotoksin nije bio učinkovit. U kasnijim fazama djelovanja β- bungarotoksina, opaža se uništavanje vezikula acetilkolinom do njihovog potpunog nestanka. Također je zabilježena vakuolizacija mitohondrija završetaka motornih živaca. Akcijski β- bungarotoksin sličan je djelovanju botulinum toksina, koji također utječe na mehanizam oslobađanja acetilkolina iz živčanih završetaka. Međutim, postoje razlike: botulinum toksin ne uzrokuje početno povećanje PEP-a; za razliku od toksina botulizma β- bungarotoksin stupa u interakciju samo s kolinergičkim završecima; Pod djelovanjem botulinum toksina nisu uočene promjene u presinaptičkom području. Sposobnost je otkrivena na sinaptosomima iz mozga štakora β- bungarotoksin smanjuje nakupljanje GABA, serotonina, norepinefrina i kolina. Jer β- Bungarotoksin uglavnom istiskuje već nakupljene neurotransmitere, može se pretpostaviti da je njegovo djelovanje povezano s oštećenjem procesa skladištenja, a ne transporta medijatora. Zaključak Mehanizam djelovanja zmijskih otrova znanstvenici još nisu u potpunosti dešifrirali. Ali prozirna kapljica otrova, jednom u krvi, širi se cijelim tijelom i, u određenoj dozi, ima blagotvoran učinak na tijelo pacijenta. Utvrđeno je da male količine otrova kobre imaju analgetski učinak te da se čak mogu koristiti kao zamjena za morfij kod pacijenata oboljelih od zloćudnih novotvorina. Štoviše, za razliku od morfija, zmijski otrov djeluje duže i, što je najvažnije, ne izaziva ovisnost. Osim toga, stvoreni su lijekovi na bazi otrova kobre koji poboljšavaju opće stanje pacijenata koji boluju od bronhijalne astme, epilepsije i angine pektoris. Potreba za zmijskim otrovom raste iz godine u godinu, a rasadnici zmija osnovani u nizu krajeva naše zemlje još ne mogu zadovoljiti tu potrebu. Stoga je potrebno zaštititi zmije otrovnice u prirodnim uvjetima, kao i osigurati njihovo razmnožavanje u zatočeništvu. Treba imati na umu da u rukama neiskusnih ljudi zmijski otrov ne postaje saveznik u borbi za očuvanje zdravlja, već opasan neprijatelj i može izazvati ozbiljno trovanje. Theophrastus Paracelsus je govorio o potrebi pravilnog odabira doze ljekovite tvari, tvrdeći da je “...sve je otrov, ništa nije lišeno otrova i sve je lijek. Sama doza čini tvar otrovom ili lijekom.” Ova izreka slavnog znanstvenika ni danas nije izgubila smisao, a pri korištenju zmijskih otrova pacijenti su dužni strogo se pridržavati uputa liječnika. Poznato je da su zmijski otrovi opasni za mnoge vrste sisavaca. Ali među niže organiziranim životinjama, osobito među kukcima, poznate su vrste koje nisu osjetljive na djelovanje zmijskog otrova, što im omogućuje da se koriste kao protuotrovi. Rezimirajući razmatranje niza pitanja koja pokrivaju značajke kemijske strukture i mehanizama djelovanja otrova, nemoguće je ne spomenuti da je priroda - ovaj najvještiji eksperimentator - dala istraživačima jedinstvene alate za proučavanje temeljnih pitanja strukture i funkcioniranje žive stanice. Zootoksini su izvrsni modeli za molekularnu biologiju, omogućujući rješavanje pitanja odnosa strukture i funkcije u biomolekulama. Bibliografija 1. Orlov B. N. “Otrovne životinje i biljke SSSR-a.” M.: Viša škola, 1990. - 272 s. G.I. Oxendendler “Otrovi i protuotrovi” L.: Nauka, 1982. - 192 str. E. Dunaev, I. Kaurov “Gmazovi. Vodozemci." M.: Astrel, 2010. - 180-ih godina. B.S. Tuniev, N.L. Orlov "Zmije Kavkaza". M.: Partnerstvo znanstvenih publikacija KMK, 2009. - 223 str. www.floranimal.ru http://www.ncbi.nlm.nih.gov/pubmed