외부 호흡 기능 부족을 진단합니다. 호흡 부전 증후군
인용: Shilov A.M., Melnik M.V., Chubarov M.V., Grachev S.P., Babchenko P.K. 만성 심부전 환자의 외부 호흡 기능 손상 // RMZh. 2004. 15호. P.912
심부전(HF)은 펌프처럼 신체의 대사 요구(기초 대사 제공)에 필요한 혈액량(MOV l/min)을 펌프질하는 심장의 무능력입니다. 심장의 펌핑 능력이 감소하면 저산소혈증이 발생하게 됩니다. 이는 심부전의 임상 징후의 기초가 되는 순환 부전의 초기 및 영구적 징후입니다. 중추 및 말초 저산소혈증의 중증도는 좌심실 부전 중 폐순환 정체로 인한 심인성 호흡 부전과 MOS 감소로 인한 말초 순환 장애로 인해 발생합니다(그림 1).
순환기 저산소증 산소의 조직으로의 최대 전달을 위한 말초 혈류 속도의 감소로 인해 산소의 동정맥 차이가 증가하여 청색증(감소된 헤모글로빈의 증가)으로 나타납니다. 이는 호기성 산화적 인산화의 주요 원인입니다. 다양한 기관의 세포의 미토콘드리아.
심인성 호흡 부전 - 심장의 펌핑 기능이 실패할 때 병리학적 과정에 폐가 관여한 결과로 인해 좌심방의 압력이 역행적으로 증가하고 폐 순환 혈관의 압력이 필연적으로 증가하여 형성됩니다. 모세혈관 수동폐고혈압. Starling 방정식에 따르면 폐 순환의 정수압이 증가함에 따라 미세혈관 내피를 통해 폐 간질로의 유체 여과 속도가 증가합니다. 체액이 림프계에 의해 제거되는 것보다 더 빨리 여과되면 혈관 주위 간질과 폐포 폐부종이 발생하여 폐 조직의 가스 교환 기능이 악화됩니다 (그림 2). 보상의 첫 번째 단계에서 간질압이 증가하면 J-수용체가 환기량의 증가로 자극되어 림프 유출이 증가하고 결과적으로 진행성 간질 부종 및 후속 폐포의 위험이 최소화됩니다. 홍수. 기계적 관점에서 볼 때, 폐 순환의 체액 정체는 폐 부피의 변화, 간질 부종으로 인한 폐 조직의 탄성 특성 감소, 폐포 범람 - 기능 단위로 나타나는 제한적 장애로 나타낼 수 있습니다. , 이는 함께 폐의 가스 교환 기능을 감소시킵니다. 폐활량과 확장성의 점진적인 감소는 흡입에 필요한 흉막강의 음압을 증가시키고 결과적으로 호흡 활동을 증가시켜 역학에 에너지를 제공하는 데 필요한 심박출량의 비율을 증가시킵니다. 호흡의. 동시에, 많은 연구자들은 기관지 점막의 부종과 기관지를 통한 자율 신경계의 기관지 수축 자극에 대한 민감도 증가로 인해 폐의 울혈이 원위 기도의 저항 증가에 기여한다는 것을 보여주었습니다. 세포 내 마그네슘 결핍의 배경에 대한 칼슘 이온 메커니즘 (그림 3). "칼슘 이온" 가설에 따르면, 기관지 폐쇄 메커니즘은 생화학적 매개체 방출의 "촉발"인 칼슘 대사 위반을 통해 "촉발"됩니다. 화학적 및 약리학적 물질에 의한 호흡기 자극은 비만세포, 호염기구, 기관지 평활근 세포 및 자율신경계의 신경 말단(특히 미주신경)의 세포질에서 칼슘 농도를 증가시킵니다. 그 결과, 비만세포에서 히스타민이 방출되고, 기관지 평활근이 수축되며, 신경 말단의 아세틸콜린이 증가하여 기관지 내피에 의한 기관지경련 및 점액 분비가 증가하게 됩니다. 다양한 작가들에 따르면, 다양한 기관지 폐쇄성 병리를 가진 환자의 40~60%가 세포 내 마그네슘 결핍을 경험합니다. (중환자실 환자 중 - 최대 70%) 인체에서 마그네슘은 네 번째이고 세포에서는 두 번째 (칼륨 다음으로) 양이온 농도입니다. 세포내 및 세포외 마그네슘은 세포 내부와 외부 모두에서 칼슘, 칼륨, 나트륨 및 인산염 이온의 농도와 이동을 조절하는 데 관여합니다. 동시에 보조 인자인 마그네슘은 신체의 대사 과정에 관여하는 300개 이상의 효소 반응을 활성화합니다. 마그네슘은 세포 지질과 상호 작용하고, 세포막의 완전성을 보장하며, 세포의 수축 요소에서 칼슘과 경쟁 관계를 맺고(액틴과 미오신 필라멘트의 상호 작용을 억제함) 미토콘드리아에서는 산화적 인산화 과정을 향상시킵니다. 전해질(나트륨, 칼륨, 칼슘 등)의 세포내 호메키네시스는 세포와 근형질막(Ca 펌프)의 필수 부분인 Na - K - Ca -ATPase의 활성화를 통해 마그네슘에 의해 제어됩니다. 근절막 Na-K 펌프와 근형질 세망의 Ca 펌프의 작동에는 호기성 산화적 인산화로 인해 미토콘드리아에서 생산되는 인산염 에너지의 30~40%가 필요합니다. 마그네슘의 세포 내 농도가 감소하면 이온 채널과 칼슘 펌프가 파괴되고 세포 내 전해질 균형이 파괴되어 세포 내부의 칼슘이 과도하게 증가하여 평활근의 수축 요소의 상호 작용이 증가합니다. 기관지의 기능과 미토콘드리아의 산화적 인산화를 억제합니다. 이러한 과정의 중단과 병행하여 마그네슘 결핍은 단백질 합성 감소(세포내 복구 억제)에 기여합니다. 1912년 Trendelenburg는 분리된 소 폐를 대상으로 한 실험에서 기관지 평활근 섬유에 대한 마그네슘 이온의 이완 효과를 입증했습니다. Hanry(1940)와 Bois(1963)의 연구에서 기니피그와 쥐를 대상으로 한 실험에서도 비슷한 결과가 얻어졌습니다. 다양한 형태의 기관지 폐쇄가 있는 환자에서 마그네슘 제제의 유사한 기관지 확장 효과가 임상 실습에서 얻어졌습니다. 최근 수십 년간의 임상 실습은 고립된 심혈관 질환의 발병 기전에서 마그네슘 결핍의 역할에 대한 집중적인 연구와 폐병리학과 결합하여 다양한 정도의 심부전 중증도 발병을 초래하는 것이 특징입니다. 축적된 임상 연구 경험에 따르면 심혈관 및 폐병리 환자 관찰의 40-70%에서 천연 및 생리학적 칼슘 길항제인 마그네슘이 결핍되어 있는 것으로 나타났습니다. 다양한 기원의 심부전 발생의 병인을 연구할 때 임상의는 전통적으로 폐쇄성 및 제한성 폐 손상으로 인한 심부전의 임상 징후 발생에서 저산소혈증의 역할을 고려하지 않고 중추 및 말초 혈역학 장애에 중점을 둡니다. 심장의 펌핑 활동이 손상됩니다. 위의 모든 사항은 다양한 기원의 CHF 환자의 외부 호흡 기능을 연구하는 이유가 되었으며, 그 결과가 이 연구에 제시되어 있습니다.
재료 및 연구 방법
100명을 검사했습니다. 즉, 실질적으로 건강한 사람 20명(대조군, 관상동맥질환 환자 40명, 다양한 정도의 CHF가 있는 COPD 환자 40명)이었습니다. 심부전의 정도와 기능분류(6분간 걷는 동안의 거리(미터))는 2001년 심부전학회(HFS)가 제안한 분류에 따라 결정하였다. COPD의 진단은 2001년 GOLD 프로그램에서 제시된 제안을 바탕으로 이루어졌습니다. COPD는 2년의 질병 병력에 걸쳐 반복적으로 3개월 동안 가래를 생성하는 기침이 존재하고 이 병리의 발병에 기여하는 위험 요소(흡연, 소아 및 청소년기의 빈번한 호흡기 감염)가 존재하여 진단되었습니다. ). 대조군 - 환자 20명, 실질적으로 건강한 45세~58세(평균나이 54.4±2.1세) - 남자 14명, 여자 6명. 스터디 그룹 1 - 관상동맥질환 환자 40명 : 50~65세(평균연령 - 58.6±4.1세)의 죽상동맥경화증 환자(29명) 또는 경색후 심근경화증 환자(11명) 중 남성이 31명, 여성이 9명이다. 이 연구에는 II A 및 II B 단계, II-III FC CHF 환자가 포함되었습니다. 일반적으로 II A st의 연구 그룹의 경우. 2기 B기 환자는 24명이었다. - 환자 16명. 처음에 CHF의 FC는 스트레스 테스트를 통해 결정되었습니다. 숨가쁨이 시작되기 6분 전에 정상적인 속도로 진행되는 거리입니다. FC II - 300m에서 425m 이하; III FC - 150m에서 300m 이하 스터디 그룹 2 - 50~60세(평균 연령 - 57.7±3.9세)의 기관지폐계 염증 기간 외의 다양한 형태의 관상동맥 질환과 CHF가 결합된 COPD 1~2기(스피로그래피에 따른) 환자 40명 남성은 28명, 여성은 12명입니다. 일반적으로 연구군에는 CHF II A 단계의 환자가 2명 있었습니다. II B기 환자는 22명이었습니다. - 환자 18명. COPD 환자 중 13명에서는 경색후 심장경화증(32.5%), 죽상동맥경화성 심장경화증의 형태로 허혈성 심장질환이 동반된 환자가 27명(67.5%)이었습니다. COPD 환자 35명(87.5%)의 흡연 기간은 평균 24.5±4.1년이었다. 연구 프로그램에 포함된 모든 환자는 치료 시작 전과 치료 후 퇴원하기 전에 ECG, 심장초음파검사, P-그래픽, 폐활량 측정 연구 및 혈액의 산-염기 균형 평가를 받았습니다. 평균 입원 기간은 21.4±2.7일이었다. 표준 요법(ACEI, 항혈소판제)을 배경으로 한 연구 그룹 1(CHF가 있는 IHD) 환자는 병원에서 심장배당체를 받았습니다. 첫 번째 단계에서는 처음 2~3일 동안 하루 0.5ml의 우아바인 정맥 주입, 그런 다음 퇴원할 때까지 - 디곡신 0.125mg을 하루 1-2회(환자 20명 - 하위군 A). CHF가 있는 관상동맥 질환 환자 20명(하위군 B)에서 이 치료법에 마그네슘 제제를 추가했습니다. Cormagnesin 10% 2g/일 정맥 주사한 다음 Magnerot 1일 1-2g 경구 투여했습니다. 연구 그룹 2(CHF가 있는 COPD)의 환자는 위에서 설명한 방법에 따라 거담제, 감작제, 강심배당체를 첨가한 점액용해제를 포함한 계획된 치료를 받았습니다(환자 20명 - 하위 그룹 A). CHF가 있는 20명의 COPD 환자(하위군 B)에서 천연 칼슘 길항제인 마그네슘 제제가 계획된 치료법에 추가되었습니다. COPD 환자 그룹에서? 2-작용제(포르모테롤)는 연구 프로그램에 포함되기 2일 전에 중단되었습니다. 치료 프로그램에 따라 연구군(CHF가 있는 IHD)과 비교군(CHF가 있는 COPD)의 환자는 동일한 수의 20명의 환자로 두 개의 하위 그룹으로 나뉘었습니다. 하위 그룹 A - 마그네슘 약물을 사용하지 않는 치료, 하위 그룹 B - 마그네슘 약물을 사용하는 치료 마그네슘 약물(Cormagnesin 10% 20 ml IV, Magnerot 정제) 첨가(표 1). 심부전 환자의 외호흡 기능에 대한 연구는 IHD와 COPD에서 폐 호흡 역학의 변화 특성을 확인하기 위해 수행되었으며 그 결과는 표 2에 나와 있습니다. 표에 따르면, HF가 합병된 IHD 및 COPD 환자의 경우 대조군에 비해 정적(VC) l) 및 동적(FVC, FEV1, l) 폐용적이 감소했습니다. 관상동맥 질환 환자 그룹에서 , VC, FVC, FEV1은 각각 48.4%, 46.5%, 48.3% 감소했습니다(p<0,01); в группе больных ХОБЛ - на 26,5%, 59% и 61,4% соответственно (р<0,001). Более выраженное снижение ЖЕЛ у больных ИБС, осложненной СН, свидетельствует о преимущественнорестриктивном характере патологии (застой в малом круге кровообращения). При анализе показателей, характеризующих проходимость воздухоносных путей, выявлена следующая особенность: в группе больных ИБС ОФВ1/ФЖЕЛ %, МОС 25-75 и ПСВ снижены соответственно на 3,2%, 4,3% и 13,8% (статистически достоверно по первому порогу вероятности безошибочного прогноза - р<0,05) по сравнению с контрольной группой; в группе больных ХОБЛ аналогичные параметры снижены на 6,1%, 39,2% и 37,8% соответственно (р<0,05±0,01). Данные показатели исследования свидетельствуют о преимущественном COPD 환자의 큰 기도 손상의 폐쇄성 (MVR 25-75, l/s 39.2% 감소), 관상동맥 질환 환자의 경우 외부 호흡 기능 장애는 복합적 성격을 띤다. 즉, 소기관지가 우세하게 포함된 제한성 폐쇄성(VC 26.5% 감소, FEV1/FVC%가 3.2% 감소했습니다. 표 3은 대조군과 HF가 있는 IHD 및 COPD 환자 그룹의 혈액의 가스 조성 및 산-염기 균형에 대한 초기 연구 결과를 나타냅니다. 표에서 볼 수 있듯이, 대조군과 검사를 받은 환자 그룹 사이의 혈액의 산소 운반 기능에는 통계적으로 유의미한 차이가 없습니다. 대조군의 Hb - 134.6±7.8 g/l, 다음 환자 그룹 허혈성 심장 질환 - 129.4±8, 1g/l, COPD 환자 그룹에서 - 138.6±6.8(p>0.05). 연구 대상 환자군 중 동맥혈의 가스 조성에서도 통계적으로 유의미한 차이는 없었습니다(p>0.05). 정맥혈의 가스 조성에 통계적으로 유의미한 차이가 대조군과 검사 대상 환자 그룹 사이에 나타났습니다. 정맥혈의 산소 분압 - PbO2 mm Hg. 관상동맥질환 환자 그룹에서는 대조군에 비해 35.8%, COPD 환자 그룹에서는 17.6% 감소했습니다(p<0,01); парциальное давление углекислого газа - РвСО2 мм рт.ст. увеличено в группе больных ИБС на 10,7%, в группе больных ХОБЛ - на 12,1% (p<0,05). Насыщение и концентрация кислородом венозной крови значительно уменьшены у больных ИБС и ХОБЛ по отношению к контрольной группе: SO2% вен. и КО2 вен. мл/дл в группе больных ИБС снижены соответственно на 43,2% и на 44,7%; в группе больных ХОБЛ - на 40,9% и на 38,8% соответственно (р<0,01). В наших исследованиях функции внешнего дыхания и газового состава артериальной и венозной крови, ЦГ до лечения у больных ИБС (40 пациентов) и ХОБЛ (40 больных), осложненных СН, согласно стадийной классификации ХСН и ФК были получены следующие результаты: - у больных ИБС до лечения нарушения функции внешнего дыхания носят смешанный характер, с преимущественным рестриктивным (застой) поражением легкого; - у больных ХОБЛ нарушения функции внешнего дыхания до лечения также имеют сочетанный характер, но преимущественно с обструктивными процессами в дыхательных путях легкого. Данные выводы основаны на результатах исследования статических, динамических объемов легкого и параметров проходимости крупных и мелких бронхов дыхательных путей: так, в группе больных ИБС ЖЕЛ и ФЖЕЛ были снижены по отношению к контрольным величинам (контрольная группа здоровых - 20 пациентов) на 48,4%, 46,5% соответственно (р<0,001), что указывает на рестриктивную патологию, вызванную застоем крови в легком; ОФВ1С, МОС 25-75 и ПСВ, характеризующие сопротивление мелких и средних бронхов (обструкция), снижены соответственно на 48,3% (р<0,001), 4,3% (р<0,05) и на 13,8% (р<0,01). Констрикция дыхательных путей в данной группе пациентов носит доклинический характер, что манифестируется отсутствием сухих хрипов на выдохе. В группе больных ХОБЛ аналогичные показатели функции внешнего дыхания: ЖЕЛ и ФЖЕЛ снижены по отношению к контрольной группе соответственно на 57,2%, 59% (р<0,01); ОФВ1С, МОС 25-75 и ПСВ л/с уменьшены соответственно на 51,4%, 39,2 и на 37,8% (p<0,01). Более выраженные изменения указанных параметров функционального состояния органов дыхания в данной группе больных, по сравнению с больными ИБС, свидетельствуют не только о застойном характере, но и документируют структурное повреждение легкого вследствие предшествующих воспалительных процессов. Нарушение насосной функции сердца, соответствующее IIА-Б стадиям и 2ФК ХСН в группах больных ИБС и ХОБЛ подтверждается снижением ФВ% по отношению к контрольной группе на 29,1%, 27,7% соответственно (р<0,01), со статистически достоверным уменьшением толерантности к физической нагрузке (ходьба 6 минут) на 39,6% в группе больных ИБС и на 41,3% в группе больных ХОБЛ (р<0,01). При анализе газового состава артериальной и венозной крови у больных ИБС и ХОБЛ с СН до лечения по сравнению с контрольной группой выявлены два компонента гипоксемии: кардиогенная дыхательная недостаточность (застой в малом круге кровообращения, обструкция воздухоносных путей) и нарушения периферического кровообращения в результате нарушения насосной функции сердца. Кардиогенная дыхательная недостаточность вследствие застоя в малом круге кровообращения и нарушения газообменной функции легкого, проявляется в наших исследованиях в виде статистически достоверного снижения оксигенации артериальной крови - PаО2 в группе больных ИБС на 15,9% (р<0,01), в группе больных ХОБЛ - на 9,7% (р<0,05) по сравнению с контрольной группой пациентов. Более выраженная разница снижения насыщения артериальной крови в группе больных ИБС по сравнению с больными ХОБЛ, возможно, вызвана большим накоплением жидкости в интерстиции легкого, снижающей диффузию кислорода, в то время как правожелудочковая недостаточность при ХОБЛ частично «разгружает» малый круг кровообращения.
저산소혈증의 순환 성분 , 말초 조직에 산소를보다 효율적으로 전달하기 위해 HF에서 말초 혈류를 보상적으로 감속시킨 결과 허혈성 심장 질환 환자 그룹에서 KEO2가 119.3 % 증가한 것으로 나타났습니다. Grad AB O2 - 155.8% 증가(p<0,001) и снижением PвО2 - на 25,8% (р<0,01); в группе больных ХОБЛ: КЭО2 увеличен на 111,2%, Grad АВ О2 - на 156,9% (р<0,01), PвО2 - снижен на 17,6% (р<0,01) по сравнению с контрольной группой.
치료 결과
심장의 펌핑 기능을 개선하면 제한적 손상이 감소하여 폐의 혈액 정체를 줄이는 데 도움이 되며, 이는 HF가 있는 관상동맥 질환 및 COPD 검사를 받은 환자의 정적 및 동적 폐용적의 증가로 우리 연구에서 확인되었습니다. 병원에서 퇴원하는 시간. 관상동맥질환 환자의 하위그룹 A에서 퇴원할 때까지 VC는 12.7%, FVC는 14%, FEV1은 15.5% 통계적으로 유의하게 증가했습니다(p<0,01), в то время как проходимость бронхиальных путей практически осталась на исходном уровне, что указывает на устранение рестриктивного компонента нарушения функции внешнего дыхания, за счет уменьшения застоя в малом круге кровообращения. В подгруппе Б (гликозиды с препаратами магния) одновременно с увеличением ЖЕЛ на 31%, ФЖЕЛ - на 23,7%, ОФВ1 - на 30,3% (p<0,001), зарегистрированыувеличения ОФВ1/ФЖЕЛ на 5,5%, МОС 25-75 - на 6,2%, ПСВ - на 4,5% (р<0,05), что указывает на устранение бронхоспастического компонента за счет бронходилатационного действия магния (рис. 1). У больных ХОБЛ в подгруппе А также отмечено увеличение исследуемых объемов легкого: VC 8.4% 증가, FVC - 15.4%, FEV1 - 14.9% 증가 (아르 자형<0,01), без динамики со стороны параметров проходимости верхних дыхательных путей. В подгруппе Б больных ХОБЛ к моменту выписки из стационара (гликозиды, препараты магния) с одновременным увеличением объемов легкого (VC 19.5% 증가, FVC - 29%, FEV1 - 40.5% 증가 , R<0,001) отмечено статистически достоверное улучшение проходимости бронхов: FEV1/FVC 8.3%% 증가, MOS 25-75 - 28.6%, PEF - 34.2% 증가 (아르 자형<0,01), что также подтверждает бронходилатирующий эффект препаратов магния. Как видно из рисунка 1, наилучший терапевтический эффект в показателях функции внешнего дыхания был достигнут у больных ХОБЛ, где в программу лечения СН были добавлены препараты магния, за счет устранения бронхообструктивного и рестриктивного (застой) компонентов. Компенсация нарушенных функций насосной деятельности сердца и внешнего дыхания суммарно привели к улучшению газового состава крови. В подгруппах А и Б больных ИБС, при стабильном уровне гемоглобина к моменту выписки из стационара, насыщение артериальной крови - PaO2는 각각 12.1%, 14.9% 증가했습니다. (아르 자형<0,01) с одновременным уменьшением PaCO2 8.2%, 13.6% (아르 자형<0,01), что свидетельствует об улучшении газообменной функции легкого. Улучшение периферического кровотока в результате нормализации насосной деятельности сердца в наших исследованиях документируется уменьшением GradАВО2 и КЭО2 в подгруппах А и Б больных ИБС соответственно на 9%-11% и на 25%-26% (р<0,01) (рис. 2). В подгруппах А и Б больных ХОБЛ к моменту выписки из стационара на фоне проведенной терапии отмечена статистически достоверная аналогичная динамика со стороны газового состава артериальной и венозной крови: PaO2는 9.15%, 15.4% 증가했습니다. (아르 자형<0,01), PaCO2는 6.1%, 5.6% 감소했습니다. (아르 자형<0,05); GradAVO2 및 KEO2 각기 5%-7% 및 7%-9% 감소 (아르 자형<0,05) (рис. 3). Более выраженная положительная динамика в газовом составе артериальной и венозной крови получена в подгруппах Б больных ИБС и ХОБЛ на фоне проводимого лечения СН, вследствие суммарного воздействия гликозидов (улучшение насосной функции сердца - положительный инотропный эффект) и препаратов магния (бронходилатирующий и вазодилатирующий эффекты) на дыхательную и СС системы. Улучшение газообменной функции легкого, насосной деятельности сердца, центральной и периферической циркуляции суммарно увеличили толерантность к физической нагрузке у больных ИБС и ХОБЛ к концу пребывания в стационаре: в подгрупах А и Б больных ИБС толерантность к физической нагрузке (количество метров при ходьбе в течение 6 мин) статистически достоверно возросла соответственно на 9% и на 17% (р<0,01), в подгруппах А и Б больных ХОБЛ 운동 내성이 14%, 19.7% 증가했습니다. (아르 자형<0,01) (рис. 4). Рисунок 4 наглядно иллюстрирует более высокую терапевтическую эффективность комбинации сердечных гликозидов с препаратами магния за счет их суммарного воздействия на сердечно-легочную системы. В результате проведенного лечения и компенсации дыхательной и сердечной недостаточности в группе больных ИБС клинические признаки IIБ ст СН отсутствовали, в то время как до лечения они имели место в 40% наблюдений, в 50% в целом по всей группе клинические признаки СН были расценены, как I ст. с 1ФК. В группе больных ХОБЛ клинические результаты лечения в виде компенсации кровообращениятакже свидетельствовали об устранении симптомов соответствующих IIБ ст. СН (в 45% наблюдений) до лечения, с переходом в I ст. СН в 47,4% наблюдений. Подобная динамика в стадиях СН явилась результатом улучшения насосной деятельности сердца, улучшения газообменной функции легкого и улучшения периферического кровообращения, что было представлено выше. Таким образом, все вышеизложенное позволяет предположить, что при развитии клинических признаков СН в результате несостоятельности насосной деятельности сердца, необходимо учитывать рестриктивные (застой крови в легком - отек интерстиция и «наводнение» альвеол) и обструктивные (бронхоспазм) компоненты нарушения функции внешнего дыхания, ведущие к снижению газового обмена и кислородо-транспортной роли крови, с нарушениями периферического кровообращения. Выраженность этих нарушений определяет стадии СН и ФК. Включение в программу лечения препаратов магния способствует более эффективному купированию клинических признаков СН с переводом в менее тяжелую стадию СН, за счет удаления застоя в легком и снятия бронхообструкции. Улучшение насосной деятельности сердца, газообменной функции легкого суммарно улучшают периферический кровоток и передачу кислорода перфузируемым органам, что документируется увеличением толерантности к физическим нагрузкам.
문학
1. Aisanov Z.R., Kokosov A.N., Ovcharenko S.I. 및 기타 만성 폐쇄
활동성 폐 질환. 연방 프로그램 // Consilium
medicum.-2002.-2권-1호
2. Belenkov Yu.N. 만성 심부전의 분류
ness // 심장마비.-2001.-vol.2.-no.6.-p. 249-250
3. Belousov Yu.B., Moiseev V.S., Lepakhin V.K. 임상약리학
지아 및 약물요법. 제 14 장. 사용되는 의약품
기관지폐쇄성 폐질환의 경우
4. Bessonova L.O., Khomyakova S.G. 전국질병회의
호흡 기관. 모스크바, 2002년 11월 11-15일. 치료에 사용된 황산마그네슘
노인 COPD 연구소 // 호흡기내과, 2002
5. Bijani H., Moghadamnia A.A., Islami Khalili E. 정맥 투여
중증 기관지 천식 환자 치료에서 황산마그네슘의 변화
tmoy, 전통적인 치료법에 반응하지 않음 // Pulmonology 2003,
13권 6호
6. Vertkin A.L., Vilkovyssky F.A., Gorodetsky V.V. mag의 응용
심장학에서의 tion 및 orotic acid // 방법론적 권장 사항.
모스크바, 1997
7. GOLD - COPD에 관한 새로운 국제 프로그램 // Russian Medi-
청저널.-2001.-12.-No.4.-P.509
8. 드보레츠키 L.I. 감염 및 만성폐쇄성폐질환
kih // Consilium medicum.-2001.-t. 3-No.12.-S. 587-594
9. 오브차렌코 S.I., 리트비노바 I.V., 레쉬첸코 I.V. 치료 알고리즘
만성 폐쇄성 폐질환 환자 // Russian Medi-
청저널.-2004
10. 오브차렌코 S.I., 레쉬첸코 I.V. 현대 진단 문제
만성 폐쇄성 폐 질환 // Russian Medical
Journal.-2003.-Vol.11.-No.4.-P.160-163
11. Svyatov I.S. 허혈성 질환 예방 및 치료에 마그네슘
심장과 그 합병증도 마찬가지입니다. 의사. 논문, 1999.
12. Shmelev E.I. 만성 폐쇄성 폐질환 // 폐
Nology, 선정된 이슈.-2001.-No.2.-S. 1-9
13. 알투라 BM, 알투라 BT. 마그네슘 이온과 혈관 수축
평활근: 일부 혈관 질환과의 관계. Fed Proc 1981;
40:2672-9
14. Brunner EH, Delabroise AM, Haddad ZH: 비경구 마그네슘의 효과
기관지 천식의 폐 기능, 혈장 cAMP 및 히스타민에 관한 것입니다. 제이
천식 1985. 22:3-11
15. Buller NP, Poole-Wilson PA. 환기 증가 메커니즘
만성심부전 환자의 운동에 대한 반응. 브르하트J
1990;63:281-283
16. Dominguez LJ, Barbagallo M, Di Lorenzo G 외. 기관지 반응성과
세포내 마그네슘: 기관지 확장의 가능한 메커니즘
천식에 마그네슘이 미치는 영향. 임상과학 1998; 95:137-142
17. Fiaccadori E, Del Canale S, Coffrini E, 외. 폐중환자실 환자의 근육 및 혈청 마그네슘. 중환자 치료 메드
1988;16:751-60.
잔여 부피와 함께, 즉 가장 깊게 숨을 내쉰 후 폐에 남아 있는 공기의 양, 폐활량은 총 폐활량(TLC)을 형성합니다. 일반적으로 폐활량은 전체 폐활량의 약 3/4이며 사람이 호흡 깊이를 변경할 수 있는 최대량을 나타냅니다. 조용한 호흡 중에 건강한 성인은 폐활량의 작은 부분을 사용합니다. 즉, 300-500ml의 공기(소위 일회 호흡량)를 흡입하고 내뿜습니다. 이 경우 흡기 예비량, 즉 사람이 조용히 들이마신 후 추가로 흡입할 수 있는 공기의 양과 조용히 숨을 내쉰 후 추가로 내쉬는 공기의 양과 동일한 예비 호기량은 각각 평균 약 1500ml입니다. 신체 활동 중에는 흡입 및 호기 매장량을 사용하여 일회 호흡량이 증가합니다.
폐활량은 스피로그래피(Spirography)를 사용하여 결정됩니다. 폐활량의 가치는 일반적으로 사람의 성별과 나이, 체격, 신체 발달에 따라 달라지며 다양한 질병에서 크게 감소하여 환자의 신체 활동에 적응하는 능력이 저하될 수 있습니다. 폐활량의 개별 값을 평가하기 위해 실제로는 이를 다양한 경험적 공식을 사용하여 계산되는 소위 적절한 폐활량(VC)과 비교하는 것이 일반적입니다. 따라서 대상의 키(미터)와 나이(B)를 기준으로 VEL(리터)은 다음 공식을 사용하여 계산할 수 있습니다. 남성의 경우 VEL = 5.2×키 - 0.029×H - 3.2; 여성용 VEL = 4.9×키 - 0.019×H - 3.76; 키가 1 ~ 1.75m 인 4 ~ 17 세 소녀의 경우 VEL = 3.75 × 높이 - 3.15; 키가 1.65m 이하인 같은 나이의 소년의 경우 VEL = 4.53 × 키 - 3.9, 키가 1.65m 이상 - VEL = 10 × 키 - 12.85입니다.
어느 정도 필요한 VC 값을 초과하는 것은 표준에서 벗어난 것이 아닙니다. 체육 및 스포츠(특히 수영, 복싱, 운동)에 관련된 신체적으로 발달한 개인의 경우 개별 VC 값이 때때로 VC를 30% 이상 초과합니다. . VC의 실제 가치가 VC의 80% 미만인 경우 VC는 감소된 것으로 간주됩니다.
폐의 폐활량 감소는 호흡기 질환 및 흉강 부피의 병리학 적 변화에서 가장 자주 관찰됩니다. 많은 경우 이는 호흡 부전(호흡 부전) 발생의 중요한 병인 메커니즘 중 하나입니다. 환자의 적당한 신체 활동 수행에 호흡의 상당한 증가가 동반되는 모든 경우, 특히 검사 결과 흉벽의 호흡 진동 진폭이 감소하고 타악기에 따라 나타나는 경우 모든 경우에 폐활량 감소를 가정해야합니다. 가슴의 경우 횡경막의 호흡 운동 및/또는 높은 위치에 제한이 있습니다. 특정 형태의 병리학 증상으로 폐활량 감소는 성격에 따라 진단 가치가 다릅니다. 잔존 폐용적 증가(폐활량 구조의 용적 재분배)로 인한 폐활량 감소와 폐활량 감소로 인한 폐활량 감소를 구별하는 것이 실질적으로 중요합니다.
폐 잔량의 증가로 인해 폐의 급성 부기 (기관지 천식 참조) 또는 폐기종 (폐기종)이 형성되어 기관지 폐쇄로 폐활량이 감소합니다. 이러한 병리학적 상태의 진단에 있어 폐활량의 감소는 그다지 중요한 증상은 아니지만, 이와 함께 발생하는 호흡 부전의 발병에 중요한 역할을 합니다. 폐활량을 감소시키는 이러한 메커니즘을 사용하면 일반적으로 폐의 전반적인 통기성과 체적 용량이 감소하지 않으며 심지어 증가할 수도 있습니다. 이는 특별한 방법을 사용하여 체적 용량을 직접 측정하여 확인하고 결정합니다. 횡격막의 낮은 위치에 의한 타악기 및 폐 위의 타악기 톤 증가 ( "박스 톤"까지). » 소리), 엑스레이 검사에 따른 폐장의 확장 및 투명성 증가. 잔기량의 증가와 폐활량의 감소가 동시에 발생하면 폐의 환기 공간 부피에 대한 폐활량의 비율이 크게 감소하여 환기 호흡 부전이 발생합니다. 이러한 경우 호흡률의 증가는 폐활량 감소를 보상할 수 있지만, 기관지 폐쇄의 경우 강제 장기간 호기로 인해 그러한 보상 가능성이 급격히 제한되므로 폐색 정도가 높으면 폐활량 감소로 이어집니다. , 일반적으로 폐포의 심한 호흡 저하 및 저산소 혈증이 발생합니다. 급성 폐팽창으로 인한 폐활량 감소는 되돌릴 수 있습니다.
TLC의 감소로 인한 VC의 감소 이유는 흉막강의 용량 감소(흉곽횡경막 병리학) 또는 폐 실질 기능의 상실 및 폐 조직의 병리학적 경직성일 수 있습니다. 또는 제한적인 유형의 호흡 부전입니다. 그 발달은 기능하는 폐포 수의 감소로 인해 폐의 가스 확산 영역이 감소한 것에 기초합니다. 후자의 환기는 크게 손상되지 않습니다. 이 경우 환기 공간의 부피에 대한 폐활량의 비율은 감소하지 않지만 (잔류 부피의 동시 감소로 인해) 더 자주 증가합니다. 호흡 증가는 저탄소증의 징후와 함께 폐포의 과호흡을 동반합니다(가스 교환 참조). 흉횡격막 병리 중 VC 및 TEL의 감소는 예를 들어 복수, 비만(픽윅 증후군 참조), 대량 흉막 삼출(흉수, 흉막염, 흉막 중피종(흉막)) 및 광범위한 흉막 유착, 기흉, 심한 척추측만증. 제한적인 호흡 부전을 동반하는 폐 질환의 범위는 작으며 주로 심각한 형태의 병리학을 포함합니다: 베릴리아증을 동반한 폐섬유증, 유육종증, 함만-리치 증후군(폐포염 참조), 미만성 결합 조직 질환(미만성 결합 조직 질환), 뚜렷한 국소 확산 폐렴 (Pneumosclerosis), 폐 부재 (폐 절제술 후) 또는 일부 (폐 절제술 후).
TLC의 감소는 폐 제한의 주요하고 가장 신뢰할 수 있는 기능적 진단 증상입니다. 그러나 의원이나 지방병원에서는 거의 사용되지 않는 특별한 장비가 필요한 TLC를 측정하기 전, 제한호흡장애의 주요 지표는 TLC 감소에 따른 폐활량 감소이다. 후자는 기관지 폐쇄의 뚜렷한 장애가 없을 때 폐활량 감소가 감지되는 경우뿐만 아니라 폐의 전체 공기 용량 감소 징후와 결합되는 경우 (타진 및 엑스레이 검사) 및 폐 아래쪽 경계의 높은 위치. 환자에게 짧고 어려운 흡입과 증가된 호흡수에서의 빠른 호기로 인해 제한되는 흡기 호흡곤란 특징이 있는 경우 진단이 용이합니다.
폐활량이 감소한 환자의 경우 호흡 기능의 역학을 모니터링하고 치료를 평가하기 위해 일정 간격으로 측정을 반복하는 것이 좋습니다.
강제 폐활량(강제 폐활량)도 참조하세요.
최대 흡입 후 생성된 최대 호기 동안 기도에서 나가는 공기의 양인 외부 호흡의 지표입니다.
Due(DEL) - 실제 생명 가치를 평가하기 위해 계산된 지표입니다. l., 특별한 공식을 사용하여 피험자의 나이와 키에 대한 데이터로부터 결정됩니다.
강제 (FVC) - J. e. l. 가능한 가장 빠른 호기로 결정됩니다. 일반적으로 90-92% F입니다. e. l., 일반적인 방법으로 결정됩니다.
다른 사전에서 폐활량의 의미 보기
1. 어떤 것을 일정량 담는 능력. 용량. E. 선박. 3리터 병. 우주비행사의 음식은 튜브에 포장되어 있습니다.
쿠즈네초프의 설명 사전
운영: 1. 일반사항
특정 시장에서 이용 가능한 보험 보장 금액(예:
지역, 국가 또는 세계) 보험 유형별 또는
문서 용량, 정보 - 의미론적 설명자(단어 및 구문)의 가중치 합계를 기반으로 계산된 문서에 포함된 정보의 양입니다.
땅의 상태를 악화시키지 않고 스스로 먹을 수 있는 가축.
운영: 1. 잠재적 보험
일반적으로 전문화되지 않은 보험사의 특정 유형의 보험 활동에 대한 역량.
특정 판매량
특정 기간 동안 시장에 판매되는 상품
에 따라 기간
상품 수요, 가격 수준, 일반 조건.
시장 용량 화폐 - 시장에서 제공되는 화폐가 흡수할 수 있는 화폐의 양을 반영하는 가치
서비스; 서비스 규모와 생산 수준에 따라 제한됩니다.
저장 용량 - 제조 창고에서 가능한 최대 저장 공간입니다.
보험 시장 수용력 - 특정 기간(보통 1년) 동안의 보험 상품 판매 규모입니다.
상품 시장의 용량은 물리적 또는 가치 측면에서 해당 연도 동안 시장에서 판매된 상품의 양입니다.
Market Money Capacity는 시장에서 제공되는 상품, 증권 및 서비스가 흡수할 수 있는 금액을 반영하는 값입니다. 서비스 규모와 생산 수준에 따라 제한됩니다.
시장 용량 - 특정 조건 및 특정 기간 동안 상품에 대한 총 소비자 수요(1995년 12월 14일자 무역부 명령 N 80)
특정 생활 상황은 특정 범죄의 시공간적 목표와 개인적 상황을 포함하여 범죄 행위 메커니즘의 요소입니다.
대형 의학사전
폐의 방선균증 - (a. 폐) 흉부 A.의 한 형태로 폐에 침윤이 발생하는 것을 특징으로 하며 일반적으로 누공 형성과 함께 안정 및 부패가 진행됩니다.
대형 의학사전
인공 환기 장치 - (동의어: A. 호흡, A. 인공 호흡, 인공 호흡기) A. 강제 환기를 통해 폐의 제어 또는 보조 인공 환기를 수행합니다.
대형 의학사전
폐 아스페르길루스증 - (a. 폐) 내장 A. 폐 손상, 객혈, 폐출혈 및 아스페르길루스종 형성으로 나타납니다.
대형 의학사전
폐 분아균증 - (b. 폐) 내장 형태의 길크리스트 분아균증의 폐 손상으로, 폐 조직이 괴사되고 화농되는 경향이 있는 국소 폐렴의 특성을 갖습니다.
대형 의학사전
어려운 생활 상황 - 시민의 삶을 객관적으로 방해하는 상황(장애, 노령으로 인한 자기 관리 불가능, 질병, 고아).
갈색 폐 압축 - (induratio fusca pulmonum: 동의어 갈색 폐 경결) 철 함유 갈색 색소가 풍부하고 집중적으로 침전되어 있는 폐 내 결합 조직의 확산 확산입니다.
대형 의학사전
대형 의학사전
폐 환기 인공 - (동의어 인공 호흡) 공기 또는 기타 가스 혼합물을 폐로 그리고 다시 환경으로 주기적으로 인위적으로 이동시켜 체내 가스 교환을 유지하는 방법입니다.
대형 의학사전
대형 의학사전
대형 의학사전
폐 환기 인공 자동 - 혈액 내 일정 수준의 이산화탄소 장력을 자동으로 유지하는 폐 환기입니다.
대형 의학사전
폐 환기 인공 비동기식 - V. l. 즉, 한쪽 폐의 흡입 단계 동안 다른 쪽 폐의 호기 단계가 발생합니다.
대형 의학사전
폐 환기 인공 보조 - V. l. 그리고. 리듬은 유지되지만 자연 호흡량이 부족한 경우, 흡입 중에 추가 양의 가스 혼합물(공기)이 폐로 펌핑되는 경우.
대형 의학사전
대형 의학사전
폐 환기 인공 전기 자극 - V. l. 즉, 횡격막 신경이나 호흡 근육의 전기적 자극으로 인해 흡입이 발생하는 경우입니다.
대형 의학사전
폐 환기 최대 - (mvl) 호흡 기능 수준을 나타내는 지표로, 최대 분당 폐 환기량(즉, 호흡 운동의 최고 빈도 및 깊이)과 동일합니다.
대형 의학사전
더 많은 단어 보기:
폐활량에 대한 Wikipedia 기사 보기
전자 형태의 온라인 사전 및 백과사전. 검색, 단어의 의미. 온라인 텍스트 번역기.
만성기관지염에서 외호흡의 기능
현재 임상 호흡 생리학은 고유한 이론적 기초, 방법 및 임무를 바탕으로 가장 빠르게 발전하는 과학 분야 중 하나입니다. 다양한 연구 방법, 점점 더 복잡해지고 비용이 증가하므로 실제 의료 분야에서 채택하기가 어렵습니다. 다양한 호흡 매개변수를 연구하기 위한 많은 새로운 방법이 아직 연구 중입니다. 사용에 대한 명확한 표시나 정량적, 정성적 평가 기준이 없습니다.
실제 작업에서는 폐활량 측정법, 기압 측정법 및 잔존 폐량을 결정하는 방법이 가장 일반적입니다. 이러한 방법을 통합적으로 사용하면 상당히 많은 정보를 얻을 수 있습니다.
스피로그램을 분석할 때 일회호흡량(TV)이 평가됩니다. 즉 조용한 호흡 중에 흡입 및 호기되는 공기의 양입니다. 분당 호흡수(RR); 분당 호흡량(MOV = DO x RR); 폐활량(VC) - 사람이 최대 흡입 후 내쉴 수 있는 공기의 양. 강제 폐활량(FVC) 곡선은 높은 기록 속도에서 최대 흡기 위치에서 최대 노력으로 완전 호기를 수행할 때 기록됩니다.
FVC 곡선에서 임의의 최대 깊이와 빈도로 호흡할 때 첫 번째 1초 동안의 강제 호기량(FEV 1)과 최대 폐 환기량(MVV)이 결정됩니다. R. F. Clement는 FVC 곡선의 직선 부분의 부피를 초과하지 않고 최대 빈도로 주어진 호흡량에서 MVL을 수행할 것을 권장합니다.
기능적 잔기 용량(FRC)과 잔존 폐량(RLV)의 측정은 폐활량측정을 크게 보완하여 총 폐활량(TLC)의 구조를 연구할 수 있습니다.
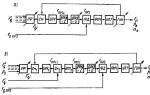
스피로그램의 개략도와 총 폐활량의 구조가 그림에 나와 있습니다.
OEL의 스피로그램 및 구조의 도식적 표현
OEL - 총 폐활량; FRC - 기능적 잔여 용량; E 공기 - 공기 용량; ROL - 잔존 폐량; 폐활량 - 폐의 폐활량; RO ind - 흡기 예비량; RO 호기 예비량; DO - 일회 호흡량; FVC - 강제 폐활량 곡선; FEV 1 - 1초간 강제 호기량; MVL - 최대 환기.
스피로그램에서는 Tiffno 지수(FEV 1 대 VC의 비율)와 풍속 지수(APSV)(MVL 대 VC의 비율)라는 두 가지 상대 지표가 계산됩니다.
얻은 지표의 분석은 센티미터 단위의 키(P)와 연령(B)을 고려하여 계산된 적절한 값과 비교하여 수행됩니다.
메모. SG 스피로그래프를 사용할 때 필요한 FEV 1은 남성의 경우 0.19l, 여성의 경우 0.14l 감소합니다. 20세 사람의 폐활량과 FEV는 25세보다 약 0.2ℓ 적습니다. 50세 이상인 경우 적정 국제 수준을 계산할 때 계수가 2만큼 감소합니다.
FRC/FLC 비율의 경우 연령에 관계없이 남녀 모두에 대해 50 ± 6%에 해당하는 일반 표준이 설정되었습니다[Kanaev N. N. et al., 1976].
TLC/TLC, FRC/TLC 및 VC의 주어진 표준을 사용하면 TLC, FRC 및 TLC의 적절한 값을 결정할 수 있습니다.
폐쇄증후군이 발생하면 절대 속도 표시기(FEV 1 및 MVL)가 VC 감소 정도를 초과하여 감소하며, 그 결과 상대 속도 표시기(FEV/VC 및 MVL/VC)가 감소하는 특징이 있습니다. 기관지 폐쇄의 심각도.
표에는 외부 호흡 지표의 편차의 정상 한계와 등급이 표시되어 있어 얻은 데이터를 올바르게 평가할 수 있습니다. 그러나 기관지 폐쇄의 심각한 장애로 인해 폐활량의 현저한 감소도 관찰되어 폐활량 측정 데이터의 해석과 폐쇄성 장애 및 혼합 장애의 구별이 복잡해집니다.
기관지 폐쇄가 심해짐에 따라 폐활량의 자연적인 감소는 B. E. Votchal 및 N. A. Magazanik(1969)에 의해 입증되고 입증되었으며, 이는 폐의 탄성 견인력 약화로 인한 기관지 내강 감소 및 기관지 내강 감소와 관련이 있습니다. 모든 폐 구조의 부피. 호기 중에 기관지 내강, 특히 세기관지가 좁아지면 기관지 저항이 증가하여 최대한의 노력을 기울여도 추가 호기가 불가능합니다.
호기 중 기관지의 내강이 작을수록 더 빨리 임계 수준으로 붕괴된다는 것이 분명합니다. 이와 관련하여 기관지 폐쇄의 심각한 장애가 있는 경우 TLC의 구조 분석이 매우 중요하며 VC의 감소와 함께 TLC의 상당한 증가가 나타납니다.
국내 저자들은 OEL 구조 분석에 큰 중요성을 부여합니다 [Dembo A. G., Shapkaits Yu. M., 1974; Kanaev N.N., Orlova A.G., 1976; Clement R.F., Kuznetsova V.I., 1976 등] FRC와 흡기 용량(E ind)의 비율은 어느 정도 조용한 호기 수준이 평형 위치에 해당하기 때문에 폐와 가슴의 탄성력 비율을 반영합니다. 이 세력의. 기관지 폐쇄가 없을 때 TLC 구조의 FRC 증가는 폐의 탄성 견인력 감소를 나타냅니다.
소기관지의 폐쇄는 TLC의 구조 변화, 주로 TLC의 증가로 이어집니다. 따라서 정상적인 스피로그램에서 TRL의 증가는 말초 기도의 폐쇄를 나타냅니다. 일반 혈량측정법을 사용하면 정상적인 기관지 저항(R aw)으로 TBL의 증가를 감지할 수 있으며 헬륨 혼합 방법을 사용하여 TBL을 결정하기 전에 작은 기관지 폐쇄를 의심할 수 있습니다[Kuznetsova V.K., 1978; KriStufek P. et al., 1980].
그러나 V. J. Sobol, S. Emirgil(1973)은 정상 수치의 큰 변동으로 인해 폐쇄성 폐질환의 조기 진단에 대한 이 지표의 신뢰성이 낮다고 지적했습니다.
기관지 폐쇄의 메커니즘에 따라 폐활량 및 속도 표시기의 변화는 고유한 특성을 갖습니다 [Kanaev N.N., Orlova A.G., 1976]. 폐쇄의 기관지경련 성분이 우세한 경우 TLC는 증가하지만 TLC의 증가에도 불구하고 폐활량은 속도 지표에 비해 약간 감소합니다.
호기시 기관지 붕괴가 우세하면 TLC가 크게 증가하며 일반적으로 TLC의 증가를 동반하지 않아 속도 표시기의 감소와 함께 VC가 급격히 감소합니다. 따라서 우리는 기관지 폐쇄의 특성으로 인한 환기 장애의 혼합 버전의 특성을 얻습니다.
환기 문제의 성격을 평가하려면 다음 규칙이 적용됩니다.
환기 문제에 대한 옵션을 평가하는 데 사용되는 규칙 [Kanaev N.N., 1980에 따름]
평가는 표준 편차의 등급에 따라 더 큰 정도로 감소되는 지표에 따라 이루어집니다. 제시된 옵션 중 처음 두 가지는 만성 폐쇄성 기관지염에서 더 흔합니다.
기압측정법(PTM)을 사용하면 최대(최대) 공기 흐름 속도가 결정되며, 이를 흡입 및 호기의 기압측정 능력(M 및 M in)이라고 합니다. 연구 결과가 매우 다양하고 많은 요인에 따라 달라지기 때문에 PTM 지표를 평가하는 것은 어렵습니다. 적절한 값을 결정하기 위해 다양한 공식이 제안되었습니다. G. O. Badalyan은 필수 M을 1.2 필수 용량, A. O. Navakatikyan - 1.2 필수 필수 용량과 동일하게 고려할 것을 제안합니다.
PTM은 환기 장애 정도를 평가하는 데 사용되지 않지만, 시간이 지남에 따라 환자를 연구하고 약리학적 테스트를 수행하는 데 중요합니다.
폐활량 측정법 및 공기압 측정법의 결과를 바탕으로 여러 가지 다른 지표가 결정되었지만 널리 사용되지는 않았습니다.
Gensler 공기 흐름 속도 지수: MVL 대 적절한 MVL의 비율, %/적절한 폐활량에 대한 폐활량의 비율, %.
Amatuni 지수: Tiffno 지수/폐활량에 대한 폐활량의 비율, %.
스피로그램 FEV 1/VC 및 FEV 1/VC의 분석에서 얻은 지표에 해당하는 지표 Mvyd/VC 및 Mvyd/VC[Amatuni V.G., Akopyan A.S., 1975].
M eq FEV 1의 감소와 R의 증가는 대형 기관지(처음 7~8세대)의 손상을 특징으로 합니다.
"만성 비특이적 폐질환"
N.R.Paleev, L.N.Tsarkova, A.I.Borokhov
기관지 말초 부분의 고립된 폐쇄를 식별하는 것은 호흡의 기능적 진단에서 중요한 문제입니다. 왜냐하면 현대 개념에 따르면 폐쇄 증후군의 발병은 말초 기관지 손상으로 정확하게 시작되고 이 단계의 병리학적 과정은 다음과 같습니다. 여전히 되돌릴 수 있습니다. 이러한 목적을 위해 폐탄성도의 빈도 의존성 연구, 용적 등 다양한 기능적 방법이 사용됩니다.
만성 기관지염의 경우, 원칙적으로 일반 방사선 사진에서는 기관지의 실제 손상을 나타내는 증상을 감지하는 것이 불가능합니다. 이러한 부정적인 방사선 데이터는 기관지 벽의 염증 변화가 이전에 방사선 사진에서 보이지 않았던 기관지를 눈에 띄게 만드는 데 충분하지 않음을 나타내는 형태학 연구에 의해 확인됩니다. 그러나 많은 경우에 다음과 관련된 방사선학적 변화를 식별하는 것이 가능합니다.
폐장의 투명도가 광범위하게 증가하는 것은 폐기종의 가장 중요한 방사선학적 징후로 간주됩니다. B. E. Votchal(1964)은 이 증상이 극도로 주관적이어서 신뢰성이 극도로 낮다는 점을 강조했습니다. 이와 함께 큰 기종성 수포와 폐의 개별 부위에 국소적으로 뚜렷한 부기가 감지될 수 있습니다. 직경이 3~4cm를 넘는 큰 기종성 수포는 투명도가 제한된 제한된 영역처럼 보입니다.
폐고혈압과 만성 폐성심이 발생하면 특정 방사선학적 징후가 나타납니다. 그 중 가장 중요한 것은 작은 말초 혈관의 구경이 감소한다는 것입니다. 이 증상은 폐포 저산소증과 저산소혈증으로 인한 전신 혈관 경련의 결과로 발생하며 폐순환 장애의 상당히 초기 증상입니다. 나중에 이미 나타난 폐동맥의 큰 가지의 확장이 나타나며, 이는 증상을 유발합니다...
기관지 조영술 검사는 만성 기관지염 진단 가능성을 크게 확장합니다. 만성 기관지염 징후의 발견 빈도는 질병의 지속 기간에 따라 다릅니다. 질병 기간이 15년 이상인 환자의 경우 96.8%에서 만성 기관지염 증상이 발견됩니다[Gerasin V. A. et al., 1975]. 기관지 조영술 검사는 만성 기관지염의 필수는 아니지만 진단에 매우 중요합니다.
의사에게 물어보세요!
질병, 상담, 진단 및 치료
외부 호흡 기능: 연구 방법
(FVD)는 폐질환의 도구 진단의 주요 영역 중 하나입니다. 여기에는 다음과 같은 방법이 포함됩니다.
더 좁은 의미에서 물리적 기능에 대한 연구는 전자 장치인 스피로그래프를 사용하여 동시에 수행되는 처음 두 가지 방법으로 이해됩니다.
우리 기사에서는 나열된 연구에 대한 적응증, 준비 및 얻은 결과의 해석에 대해 이야기할 것입니다. 이는 호흡기 질환 환자가 특정 진단 절차의 필요성을 이해하고 얻은 데이터를 더 잘 이해하는 데 도움이 될 것입니다.
우리의 호흡에 대해 조금
호흡은 신체가 생명에 필요한 공기로부터 산소를 받고 신진대사 중에 형성되는 이산화탄소를 방출하는 중요한 과정입니다. 호흡에는 외부 (폐 참여), 적혈구 및 조직에 의한 가스 전달, 즉 적혈구와 조직 간의 가스 교환 단계가 있습니다.
맥박 산소 측정 및 혈액 가스 분석을 사용하여 가스 전달을 연구합니다. 또한 우리 주제에서 이러한 방법에 대해 조금 이야기하겠습니다.
폐의 환기 기능에 대한 연구가 가능하며 호흡기 질환에 대해 거의 모든 곳에서 수행됩니다. 이는 호흡 중 폐용적과 공기 유량 측정을 기반으로 합니다.
조수량 및 용량
폐활량(VC)은 가장 깊게 흡입한 후 내쉬는 최대 공기량입니다. 실제로 이 볼륨은 심호흡 중에 얼마나 많은 공기가 폐에 "적합"하고 가스 교환에 참여할 수 있는지 보여줍니다. 이 지표가 감소하면 제한적 장애, 즉 폐포의 호흡 표면 감소를 나타냅니다.
기능적 폐활량(FVC)은 폐활량과 마찬가지로 측정되지만 빠르게 호기하는 동안에만 측정됩니다. 그 값은 빠른 호기가 끝날 때 기도의 일부가 붕괴되어 폐포에 특정 양의 공기가 "숨을 쉬지 않은"상태로 남아 있기 때문에 폐활량보다 적습니다. FVC가 VC보다 크거나 같으면 테스트가 잘못 수행된 것으로 간주됩니다. FVC가 VC보다 1리터 이상 적다면 이는 너무 일찍 허탈되어 공기가 폐에서 빠져나가는 것을 막는 작은 기관지의 병리를 나타냅니다.
빠른 호기 동작을 수행하는 동안 또 다른 매우 중요한 매개변수인 1초 강제 호기량(FEV1)이 결정됩니다. 이는 폐쇄성 장애, 즉 기관지의 공기 출구가 막히는 경우, 특히 만성 기관지염 및 중증 기관지 천식에서 감소합니다. FEV1을 적절한 값과 비교하거나 폐활량 대비 비율(Tiffenau index)을 사용합니다.
Tiffno 지수가 70% 미만으로 감소하면 심각한 기관지 폐쇄가 있음을 나타냅니다.
MVL(분당 폐 환기 지표)은 분당 가장 빠르고 깊은 호흡 동안 폐를 통과하는 공기의 양을 결정합니다. 일반적으로 150리터 이상입니다.
폐기능 검사
이는 폐용적과 속도를 결정하는 데 사용됩니다. 또한 기능 테스트는 어떤 요인이 작용한 후 이러한 지표의 변화를 기록하기 위해 처방되는 경우가 많습니다.
징후 및 금기 사항
호흡 기능에 대한 연구는 기관지 폐쇄 장애 및/또는 호흡 표면 감소를 동반하는 모든 기관지 및 폐 질환에 대해 수행됩니다.
이 연구는 다음과 같은 경우 금기 사항입니다.
- 간호사의 지시를 정확하게 따르지 못하는 4~5세 미만의 어린이
- 급성 전염병 및 발열;
- 심한 협심증, 심근경색의 급성기;
- 고혈압, 최근 뇌졸중;
- 울혈성 심부전, 휴식 시 호흡곤란 및 약간의 활동을 동반함;
- 지침을 올바르게 따르지 못하게 하는 정신 장애.
연구가 수행되는 방법
절차는 기능 진단실에서 앉은 자세로, 바람직하게는 아침 공복 또는 식사 후 1.5시간 이내에 수행됩니다. 의사의 처방에 따라 환자가 지속적으로 복용하고 있는 기관지 확장제를 중단할 수 있습니다. 단기간 작용하는 베타2 작용제 - 6시간, 장시간 작용하는 베타2 작용제 - 12시간, 장기간 작용하는 테오필린 - 검사 하루 전.
폐기능 검사
환자의 코를 특수 클립으로 막아 일회용 또는 멸균 가능한 마우스피스(마우스피스)를 사용하여 입으로만 호흡이 이루어지도록 합니다. 피험자는 호흡 과정에 집중하지 않고 한동안 침착하게 호흡합니다.
그런 다음 환자는 차분한 최대 흡입과 동일한 차분한 최대 호기를 취하도록 요청받습니다. 이것이 생명력을 평가하는 방법입니다. FVC와 FEV1을 평가하기 위해 환자는 차분하고 심호흡을 하고 가능한 한 빨리 모든 공기를 내쉬십시오. 이 지표는 짧은 간격으로 세 번 기록됩니다.
연구가 끝나면 환자가 10초 동안 최대한 깊고 빠르게 호흡할 때 다소 지루한 MVL 등록이 수행됩니다. 이 기간 동안 약간 현기증을 느낄 수 있습니다. 위험하지 않으며 테스트를 중단하면 빠르게 사라집니다.
많은 환자들이 기능 검사를 처방받습니다. 가장 일반적인 것 :
- 살부타몰로 시험하고;
- 운동 테스트.
메타콜린 검사는 덜 자주 처방됩니다.
살부타몰로 테스트를 실시할 때 초기 스피로그램을 기록한 후 환자에게 경련성 기관지를 확장시키는 단기 작용 베타2 작용제인 살부타몰을 흡입하도록 요청합니다. 15분 후에 연구가 반복됩니다. M-항콜린성 이프라트로피움 브로마이드를 흡입할 수도 있으며, 이 경우 30분 후에 테스트를 반복합니다. 정량 에어로졸 흡입기를 사용하여 투여할 수 있을 뿐만 아니라 경우에 따라 스페이서나 분무기를 사용하여 투여할 수도 있습니다.
FEV1 지표가 12% 이상 증가하는 동시에 절대값이 200ml 이상 증가하면 양성으로 간주됩니다. 이는 FEV1의 감소로 나타나는 처음에 확인된 기관지 폐쇄가 가역적이며 살부타몰 흡입 후 기관지 개통성이 향상됨을 의미합니다. 이것은 기관지 천식에서 관찰됩니다.
처음에 감소된 FEV1 값에서 검사가 음성인 경우 이는 기관지를 확장시키는 약물에 반응하지 않는 비가역적인 기관지 폐쇄를 나타냅니다. 이 상황은 만성 기관지염에서 관찰되며 천식에서는 일반적이지 않습니다.
살부타몰 흡입 후 FEV1 지표가 감소하면 이는 흡입에 대한 기관지 경련과 관련된 역설적 반응입니다.
마지막으로, 초기 정상 FEV1 값의 배경에 대해 테스트가 양성인 경우 이는 기관지 과민성 또는 숨겨진 기관지 폐쇄를 나타냅니다.
부하 테스트를 실시할 때 환자는 자전거 인체공학계나 트레드밀에서 6~8분 동안 운동을 수행한 후 반복 테스트를 수행합니다. FEV1이 10% 이상 감소하면 운동 천식을 나타내는 양성 테스트를 말합니다.
호흡기내과 병원에서는 기관지 천식을 진단하기 위해 히스타민이나 메타콜린을 이용한 유발검사도 사용한다. 이 물질은 아픈 사람에게 변형된 기관지의 경련을 유발합니다. 메타콜린을 흡입한 후 반복 측정이 이루어집니다. FEV1이 20% 이상 감소하면 기관지 과민반응과 기관지 천식의 가능성을 나타냅니다.
결과는 어떻게 해석되나요?
기본적으로 실제로 기능 진단 의사는 폐활량과 FEV1이라는 두 가지 지표에 중점을 둡니다. 대부분의 경우 R. F. Clement et al.이 제안한 표에 따라 평가됩니다. 다음은 표준의 백분율을 보여주는 남성과 여성에 대한 일반적인 표입니다.
예를 들어, 폐활량이 55%이고 FEV1이 90%인 경우 의사는 정상적인 기관지 개통에도 불구하고 폐 폐활량에 상당한 감소가 있다고 결론을 내릴 것입니다. 이 상태는 폐렴 및 폐포염의 제한적 장애에 일반적입니다. 반대로 만성 폐쇄성 폐질환의 경우 폐활량은 70%(약간의 감소), FEV1 – 47%(급격한 감소)일 수 있으며, 살부타몰 검사는 음성입니다.
우리는 위에서 기관지 확장제, 운동, 메타콜린 검사의 해석에 대해 이미 논의했습니다.
외부 호흡 기능을 평가하는 또 다른 방법도 사용됩니다. 이 방법을 사용하면 의사는 강제 폐활량(FVC)과 FEV1이라는 2가지 지표에 중점을 둡니다. FVC는 가능한 한 오랫동안 지속되는 날카로운 완전 호기로 심호흡 후에 결정됩니다. 건강한 사람의 경우 이 두 지표 모두 정상의 80% 이상입니다.
FVC가 정상의 80%를 초과하고 FEV1이 정상의 80% 미만이며 그 비율(Tiffno 지수가 아닌 Genzlar 지수!)이 70% 미만인 경우 폐쇄 장애를 말합니다. 이는 주로 기관지 개통성 장애 및 호기 과정과 관련이 있습니다.
두 지표가 모두 표준의 80% 미만이고 비율이 70%를 초과하는 경우 이는 제한적 장애, 즉 완전한 흡기를 방해하는 폐 조직 자체의 병변의 징후입니다.
FVC와 FEV1의 값이 정상의 80% 미만이고 그 비율이 70% 미만인 경우 이는 복합 장애입니다.
폐색의 가역성을 평가하려면 살부타몰 흡입 후 FEV1/FVC 값을 살펴보십시오. 70% 미만으로 유지되면 장애는 되돌릴 수 없습니다. 이는 만성 폐쇄성 폐질환의 징후입니다. 천식은 가역적인 기관지 폐쇄가 특징입니다.
되돌릴 수 없는 장애가 확인되면 그 심각도를 평가해야 합니다. 이를 위해 살부타몰을 흡입한 후 FEV1을 평가합니다. 그 값이 표준의 80%를 초과하면 경미한 폐색, 50-79% – 보통, 30–49% – 심각, 표준의 30% 미만 – 심각이라고 말합니다.
폐 기능 검사는 치료 전 기관지 천식의 중증도를 결정하는 데 특히 중요합니다. 앞으로는 자가 모니터링을 위해 천식 환자가 최대 유량 측정을 하루에 두 번 수행해야 합니다.
피크 유량
이는 기도가 좁아지는 정도(폐쇄)를 판단하는 데 도움이 되는 연구 방법입니다. 최대 유량 측정은 호기 공기용 눈금과 마우스피스가 장착된 소형 장치인 최대 유량계를 사용하여 수행됩니다. 최대유량측정법은 기관지 천식의 경과를 조절하는 데 가장 널리 사용됩니다.
피크 유량 측정은 어떻게 수행됩니까?
천식이 있는 각 환자는 하루에 두 번 최대 유량 측정을 수행하고 그 결과를 일기에 기록하고 일주일 동안의 평균값을 결정해야 합니다. 또한 그는 자신의 최선의 결과를 알아야 합니다. 평균 지표의 감소는 질병 경과에 대한 통제력이 저하되고 악화가 시작되었음을 나타냅니다. 이 경우 의사와 상담하거나 폐 전문의가 사전에 방법을 설명한 경우 치료 강도를 높여야합니다.
일일 피크 흐름 차트
최고 유량 측정법은 호기 동안 달성된 최대 속도를 보여주며, 이는 기관지 폐쇄 정도와 밀접한 관련이 있습니다. 앉은 자세로 수행됩니다. 먼저, 환자는 침착하게 호흡한 다음 심호흡을 하고 장치의 마우스피스를 입술에 대고 최대 유량계를 바닥 표면과 평행하게 유지한 후 최대한 빠르고 강렬하게 숨을 내쉬게 됩니다.
이 과정은 2분 후에 반복되고, 2분 후에 다시 반복됩니다. 세 가지 지표 중 가장 좋은 것이 일기에 기록됩니다. 측정은 기상 후, 취침 전 동시에 실시됩니다. 치료 선택 기간 동안이나 상태가 악화되는 경우 낮 시간에 추가 측정을 할 수 있습니다.
데이터를 해석하는 방법
이 방법의 정상 값은 각 환자마다 개별적으로 결정됩니다. 정기적인 사용 시작 시, 질병의 완화에 따라 3주 동안 최대 호기량(PEF)에 대한 가장 좋은 지표가 발견됩니다. 예를 들어 400l/s와 같습니다. 이 숫자에 0.8을 곱하면 특정 환자에 대한 정상 값의 최소 한계인 320 l/min을 얻습니다. 이 숫자보다 높은 것은 "녹색 영역"에 있으며 천식이 잘 조절되었음을 나타냅니다.
이제 400l/s에 0.5를 곱하면 200l/s가 됩니다. 이것은 "빨간색 구역"의 상한선입니다. 이는 긴급한 치료가 필요할 때 기관지 개통성이 위험한 수준으로 감소하는 것입니다. 치료 조정이 필요할 때 200l/s에서 320l/s 사이의 PEF 값은 "노란색 영역" 내에 있습니다.
이러한 값을 자체 모니터링 그래프에 표시하는 것이 편리합니다. 이를 통해 천식이 얼마나 잘 조절되는지 알 수 있습니다. 이렇게 하면 상태가 악화될 경우 적시에 의사와 상담할 수 있으며 장기적으로 잘 관리하면 받는 약의 복용량을 점차적으로 줄일 수 있습니다(또한 폐질환 전문의가 처방한 경우에만).
맥박 산소 측정
맥박산소측정법은 동맥혈의 헤모글로빈에 의해 운반되는 산소의 양을 결정하는 데 도움이 됩니다. 일반적으로 헤모글로빈은 이 가스 분자를 최대 4개까지 포착하는 반면 동맥혈의 산소 포화도(포화도)는 100%입니다. 혈액 내 산소량이 감소하면 포화도도 감소합니다.
이 표시기를 결정하기 위해 맥박 산소 측정기와 같은 소형 장치가 사용됩니다. 그것은 손가락에 꽂는 일종의 "옷핀"처럼 보입니다. 이러한 유형의 휴대용 장치는 시중에 판매되고 있으며, 만성 폐질환을 앓고 있는 환자라면 누구나 구입하여 자신의 상태를 모니터링할 수 있습니다. 맥박 산소 측정기는 의사들에게도 널리 사용됩니다.
맥박 산소 측정은 병원에서 언제 수행됩니까?
- 산소 요법 중 효과를 모니터링하기 위해;
- 호흡 부전으로 중환자실에서;
- 심각한 외과 개입 후;
- 폐쇄성 수면 무호흡 증후군이 의심되는 경우 - 수면 중에 주기적으로 호흡을 멈추십시오.
맥박 산소 측정기를 직접 사용할 수 있는 경우는 언제입니까?
- 천식이나 기타 폐질환이 악화되는 동안 상태의 중증도를 평가하기 위해
- 수면 무호흡증이 의심되는 경우 - 환자가 코를 골거나 비만, 당뇨병, 고혈압 또는 갑상선 기능 저하가 있는 경우 - 갑상선 기능 저하증.
동맥혈의 산소포화도는 95~98%이다. 집에서 측정한 이 지표가 감소하면 의사와 상담해야 합니다.
혈액가스 연구
이 연구는 실험실에서 수행되며 환자의 동맥혈을 검사합니다. 이는 산소, 이산화탄소, 포화도 및 기타 이온의 농도를 결정합니다. 이 연구는 주로 병원, 주로 집중 치료실에서 심한 호흡 부전, 산소 요법 및 기타 응급 상황에서 수행됩니다.
요골, 상완 또는 대퇴 동맥에서 혈액을 채취 한 다음 천자 부위를 면봉으로 몇 분 동안 누르고 큰 동맥을 천자 할 때는 출혈을 피하기 위해 압박 붕대를 감습니다. 천자 후 환자의 상태를 모니터링하십시오. 시간이 지남에 따라 사지의 붓기와 변색을 확인하는 것이 특히 중요합니다. 환자는 사지의 무감각, 저림 또는 기타 불편함을 경험하는 경우 의료진에게 알려야 합니다.
정상 혈액 가스 값:
PO 2, O 2 ST, SaO 2, 즉 산소 함량의 감소와 이산화탄소 분압의 증가는 다음 조건을 나타낼 수 있습니다.
- 호흡 근육의 약화;
- 뇌 질환 및 중독의 호흡기 센터 우울증;
- 기도 폐쇄;
- 기관지 천식;
- 기종;
- 폐렴;
- 폐출혈.
동일한 지표가 감소하지만 정상적인 이산화탄소 함량은 다음 조건에서 발생합니다.
정상적인 산소압과 포화도에서 O 2 ST의 감소는 심각한 빈혈과 순환 혈액량 감소의 특징입니다.
따라서 우리는 본 연구의 수행과 결과의 해석이 매우 복잡하다는 것을 알 수 있습니다. 심각한 의료 절차, 특히 인공 환기에 대한 결정을 내리려면 혈액 가스 구성 분석이 필요합니다. 따라서 외래 환자를 대상으로 하는 것은 의미가 없습니다.
외부 호흡 기능을 연구하는 방법을 배우려면 비디오를 시청하십시오.
외부 호흡 장치의 기능은 신체에 산소를 공급하고 대사 과정에서 생성된 일산화탄소(IV)를 제거하는 것을 목표로 합니다. 이 기능은 첫째로 환기에 의해 수행됩니다. 즉, 외부 공기와 폐포 공기 사이의 가스 교환으로 폐포에 필요한 산소 및 일산화탄소(IV) 압력을 제공합니다(중요한 점은 흡입된 공기의 폐내 분포입니다). 둘째, 산소와 일산화탄소(IV)가 폐포와 폐 모세혈관의 벽을 통해 확산되어 반대 방향으로 발생합니다(산소는 폐포에서 혈액으로 흐르고 일산화탄소(IV)는 혈액에서 폐로 확산됩니다. 폐포). 기관지 및 폐의 많은 급성 및 만성 질환은 호흡 부전의 발병으로 이어지며(이 개념은 1854년 Wintrich에 의해 도입됨) 폐의 형태학적 변화 정도가 항상 기능 부전의 정도와 일치하는 것은 아닙니다.
현재 호흡 부전은 정상적인 혈액 가스 조성의 유지가 보장되지 않거나 외부 호흡 장치 및 심장의보다 집중적 인 작업을 통해 달성되어 호흡 곤란을 감소시키는 신체 상태로 정의하는 것이 일반적입니다. 신체의 기능적 능력. 외부 호흡 장치의 기능은 순환계의 기능과 매우 밀접하게 관련되어 있다는 점을 명심해야 합니다. 외부 호흡이 부족한 경우 심장 활동의 증가는 보상의 중요한 요소 중 하나입니다.
임상 적으로 호흡 부전은 호흡 곤란, 청색증 및 말기 (심부전이 추가되는 경우) 부종으로 나타납니다.
호흡기 질환 환자의 호흡 부전의 경우 신체는 힘든 육체 노동을 수행할 때 건강한 사람과 동일한 보상 예비 메커니즘을 사용합니다. 그러나 이러한 메커니즘은 건강한 사람에게 필요하지 않을 정도의 부하에서 훨씬 더 일찍 작동합니다(예를 들어, 천천히 걸을 때 폐기종 환자의 호흡 곤란 및 빈호흡이 발생할 수 있음).
호흡 부전의 첫 번째 징후 중 하나는 건강한 사람의 신체 활동이 비교적 적은 상태에서 환기의 부적절한 변화(호흡 증가, 심화)입니다. MOD가 증가합니다. 어떤 경우에는(기관지 천식, 폐기종 등) 호흡 부전에 대한 보상이 주로 호흡 근육의 활동 증가, 즉 호흡 역학의 변화로 인해 수행됩니다. 따라서 호흡기 병리학 환자의 경우 외부 호흡 기능을 적절한 수준으로 유지하는 것은 보상 메커니즘을 연결하여 수행됩니다. 건강한 개인보다 더 많은 노력을 기울이고 호흡 예비력을 제한합니다. 최대 폐 환기 ( MVV) 감소, 산소이용률(KIO 2) 등
진행성 호흡 부전과의 싸움에 다양한 보상 메커니즘을 포함시키는 것은 그 정도에 따라 점차적으로 발생합니다. 처음에는 호흡 부전의 초기 단계에서 휴식 시 외부 호흡 장치의 기능이 일반적인 방식으로 수행됩니다. 환자가 육체 노동을 수행할 때만 보상 메커니즘이 활성화됩니다. 따라서 외부 호흡 장치의 예비 능력이 감소합니다. 나중에 작은 부하와 휴식 중에 빈호흡 및 빈맥이 관찰되고 흡입 및 호기 중 호흡 근육의 작업이 증가하고 호흡 행위에 추가 근육 그룹의 참여가 결정됩니다. 호흡 부전의 후기 단계에서 신체의 보상 능력이 고갈되면 동맥 저산소혈증과 고탄산증이 감지됩니다. "명백한" 동맥 저산소증의 증가와 병행하여 "숨겨진" 산소 결핍의 징후와 혈액 및 조직에서 과소산화된 생성물(젖산 등)의 축적도 관찰됩니다.
그 후, 폐부전은 폐 순환의 고혈압 발생으로 인한 심부전 (우심실) 부전과 결합되어 심장 우심실의 부하 증가와 지속적인 심근 장애로 인한 심근 이영양증 변화를 동반합니다. 과부하 및 산소 공급 부족. 폐의 확산 병변이있는 폐 순환 혈관의 고혈압은 폐의 환기 부족, 폐포 저산소증 (Euler-Lillestrand 반사; 폐의 국소 병변의 경우)에 반응하여 반사적으로 발생합니다. 이 반사 메커니즘은 중요한 적응 역할을하여 다음을 제한합니다. 환기가 부족한 폐포에 혈액 공급).
미래에는 흉터 경화 과정 (및 폐 혈관 네트워크 손상)으로 인해 폐의 만성 염증성 질환으로 인해 폐 순환 혈관을 통한 혈액 통과가 더욱 어려워집니다. 우심실 심근에 가해지는 부하가 증가하면 점차 실패로 이어지며 전신 순환계의 혼잡(소위 폐성심)으로 표현됩니다.
호흡 부전의 원인과 메커니즘에 따라 폐쇄성, 제한성("제한적") 및 혼합형("결합")의 세 가지 유형의 폐 환기 기능 장애가 구분됩니다.
방해 유형기관지를 통해 공기가 통과하기 어려운 것이 특징입니다 (기관지염 - 기관지 염증, 기관지 경련, 기관 또는 큰 기관지의 협착 또는 압박, 예를 들어 종양 등으로 인해). 스피로그래픽 연구에서는 VC가 약간 감소하면서 MVL과 FVC가 뚜렷하게 감소하는 것으로 확인되었습니다. 공기 흐름이 막히면 호흡 근육에 대한 요구가 증가하고, 추가 기능적 부하를 수행하는 호흡 장치의 능력이 영향을 받습니다(특히 빠르게 흡입하고 특히 호기하는 능력과 호흡의 급격한 증가는 손상됨).
제한적(제한적) 유형폐의 확장 및 붕괴 능력이 제한될 때 환기 장애가 관찰됩니다: 기압 경화증, 수압 또는 기흉, 대규모 흉막 유착, 후만 측만증, 늑골 연골의 골화, 갈비뼈의 제한된 이동성 등. 이러한 조건에서 첫 번째 제한은 가능한 최대 흡입 깊이, 즉 폐활량(및 MVL)이 감소하지만 호흡 활동의 역학, 즉 일반적인 흡기 깊이의 속도에 장애가 없으며 필요한 경우 호흡량이 크게 증가합니다.
혼합(복합)형이전 유형의 두 가지 특성을 결합하며 종종 그 중 하나가 우세합니다. 장기간의 폐 및 심장 질환에서 발생합니다.
다음의 경우에도 외호흡 기능의 부족이 발생합니다. 증가하다소위 해부학적 사강(폐의 큰 구멍, 동굴, 농양 및 여러 개의 큰 기관지 확장증의 경우). 호흡부전은 이 유형에 가깝습니다. 순환 장애로 인해(예를 들어, 혈전색전증 등의 경우) 폐의 일부가 어느 정도 환기를 유지하면서 가스 교환이 차단되는 경우입니다. 마지막으로 호흡 부전은 다음과 같은 경우에 발생합니다. 폐의 공기 분포가 고르지 않음(“분포 장애”) 혈액 공급이 유지되는 경우 환기(폐렴, 무기폐)에서 폐의 일부가 제외될 때까지. 이로 인해 정맥혈의 일부가 산소화되지 않은 채 폐정맥과 심장의 왼쪽으로 들어갑니다. 이러한 유형의 호흡 부전에 병리학적으로 가까운 것은 소위 다음과 같은 경우입니다. 혈관 션트(오른쪽에서 왼쪽으로) 폐동맥 시스템의 정맥혈 일부가 모세혈관을 우회하여 직접 폐정맥으로 들어가 산소가 공급된 동맥혈과 혼합됩니다. 후자의 경우 폐 내 혈액의 산소 공급이 손상되지만 건강한 폐 부위의 환기가 보상적으로 증가하여 고탄산증이 관찰되지 않을 수 있습니다. 이는 저산소혈증과 고탄산혈증이 모두 관찰되는 완전, 전체 "실질"과는 대조적으로 부분 호흡 부전입니다.
소위 확산성 호흡부전폐의 폐포-모세혈관막을 통한 가스 교환 장애가 특징이며, 이것이 두꺼워지면 이를 통한 가스 확산 장애(소위 폐렴, "폐포-모세혈관 차단")를 유발하며 일반적으로 동반되지 않습니다. 일산화탄소(IV)의 확산 속도가 산소보다 20배 높기 때문에 저탄소증에 의해 발생합니다. 이러한 형태의 호흡 부전은 주로 동맥 저산소혈증과 청색증으로 나타납니다. 환기가 강화되었습니다.
폐 병리와 직접적인 관련이 없음 호흡 센터의 독성 저하, 빈혈, 흡입 공기의 산소 부족으로 인한 호흡 부전.
가장 밝은 부분 심각한(예를 들어, 기관지 천식, 대엽성 폐렴, 자발성 기흉 발작 중) 및 만성 호흡 부전.
호흡 부전에도 3단계와 3단계가 있습니다. 호흡 부전의 정도는 질병이 발생한 특정 순간의 심각도를 반영합니다. 1등급에서는 중등도 또는 상당한 육체적 활동 시에만 호흡 부전(주로 호흡곤란)이 감지되고, 2등급에서는 가벼운 육체적 활동 시 호흡곤란이 나타나며 휴식 시 보상 메커니즘이 이미 활성화되어 기능적 진단 방법으로 다음과 같은 증상을 확인할 수 있습니다. 적절한 값과의 편차 수. III 등급에서는 휴식 시 동맥 저산소혈증의 징후로 숨가쁨과 청색증이 관찰될 뿐만 아니라 기능적 폐 검사 매개변수가 정상과 크게 차이가 납니다.
만성 폐질환에서 호흡 부전 단계의 식별은 질병이 진행되는 동안의 역학을 반영합니다. 일반적으로 잠복 폐, 중증 폐 및 폐심부전의 단계가 구분됩니다.
치료.호흡 부전의 경우 다음과 같은 조치를 제공합니다. 1) 이를 유발한 기저 질환(폐렴, 삼출성 흉막염, 기관지 및 폐 조직의 만성 염증 과정 등)의 치료; 2) 기관지 경련 완화 및 폐 환기 개선 (기관지 확장제 사용, 물리 치료 등) 3) 산소 요법; 4) "폐심장"이 있는 경우 - 이뇨제 사용 5) 전신 순환 장애 및 증상이 있는 적혈구 증가증의 경우 추가 방혈이 수행됩니다.
사람의 흡입과 호기는 단순한 생리적 과정이 아닙니다. 다양한 생활 환경에서 우리가 어떻게 호흡하는지 기억하십시오.
두려움, 분노, 고통 - 호흡이 제한되고 제한됩니다. 행복 – 기쁨을 표현할 수 있는 감정이 충분하지 않습니다 – 우리는 깊게 숨을 쉰다.
질문에 대한 또 다른 예: 사람이 음식, 잠, 물 없이 얼마나 오래 살 수 있습니까? 그리고 공기가 없다면? 사람의 삶에서 호흡의 중요성에 대해 계속 이야기하는 것은 아마도 가치가 없을 것입니다.
호흡 - 요약 정보
 고대 인도의 요가 가르침에서는 이렇게 말합니다. “인간의 삶은 들숨과 날숨 사이의 일시적인 기간입니다. 왜냐하면 이러한 움직임은 모든 세포를 공기로 포화시켜 인간의 존재 자체를 보장하기 때문입니다.”
고대 인도의 요가 가르침에서는 이렇게 말합니다. “인간의 삶은 들숨과 날숨 사이의 일시적인 기간입니다. 왜냐하면 이러한 움직임은 모든 세포를 공기로 포화시켜 인간의 존재 자체를 보장하기 때문입니다.”
반쯤 숨쉬는 사람은 반쯤 산다. 물론 우리는 건강에 해롭거나 부적절한 호흡에 대해 이야기하고 있습니다.
의식의 참여없이 모든 일이 일어난다면 독자는 어떻게 호흡을 잘못 할 수 있습니까? 즉 "자동으로"말하자면 이의를 제기 할 것입니다. 똑똑한 사람은 계속할 것입니다. 호흡은 무조건 반사에 의해 제어됩니다.
진실은 우리가 평생 동안 축적하는 심리적 트라우마와 온갖 질병에 있습니다. 그들은 근육을 긴장(과도하게 긴장)시키거나 반대로 게으르게 만드는 사람들입니다. 따라서 시간이 지남에 따라 호흡주기의 최적 모드가 손실됩니다.
고대인은 이 과정의 정확성에 대해 생각하지 않은 것 같습니다. 자연 자체가 그를 위해 그렇게 했습니다.
인간의 장기에 산소를 채우는 과정은 세 가지 구성 요소로 나뉩니다.
- 쇄골(상부).흡입은 상부 늑간 근육과 쇄골로 인해 발생합니다. 이 기계적 움직임이 가슴을 완전히 확장시키지 않는지 확인하십시오. 산소가 거의 공급되지 않고 호흡이 잦아지고 불완전해지며 현기증이 발생하고 질식하기 시작합니다.
- 중간 또는 가슴.이 유형에서는 늑간근과 갈비뼈 자체가 활성화됩니다. 가슴은 최대로 팽창하여 공기로 완전히 채워집니다. 이 유형은 스트레스가 많은 상황이나 정신적 스트레스에서 전형적으로 나타납니다. 상황을 기억하십시오. 당신은 흥분되지만 심호흡을하자마자 모든 것이 어딘가에서 사라집니다. 이는 올바른 호흡의 결과입니다.
- 복부 횡격막 호흡.해부학적인 관점에서 볼 때 이러한 유형의 호흡이 가장 적합하지만 물론 완전히 편안하고 친숙하지는 않습니다. 정신적 스트레스 해소가 필요할 때 언제든 활용 가능합니다. 복부 근육을 이완시키고 횡경막을 가장 낮은 위치로 내린 다음 다시 시작 위치로 되돌립니다. 머리가 차분해지고 생각이 더 명확해졌습니다.
중요한! 횡격막을 움직여 호흡을 개선할 뿐만 아니라 복부 장기를 마사지하여 대사 과정과 음식 소화를 개선합니다. 횡경막의 움직임으로 인해 소화 기관으로의 혈액 공급과 정맥 유출이 활성화됩니다.
이것은 사람이 올바르게 호흡하는 것뿐만 아니라 이 과정을 보장하는 건강한 기관을 갖는 것이 얼마나 중요한지입니다. 후두, 기관, 기관지, 폐의 상태를 지속적으로 모니터링하면 이러한 문제를 해결하는 데 크게 기여합니다.
폐기능 검사
의학에서의 FVD란 무엇입니까? 외부 호흡 기능을 테스트하기 위해 다양한 기술과 절차가 사용되며, 주요 임무는 폐와 기관지의 상태를 객관적으로 평가하고 병리학 발달의 초기 단계에서 부검을 수행하는 것입니다.
폐 조직에서 혈액과 체내로 유입되는 외부 공기 사이에서 일어나는 가스 교환 과정을 의학에서는 외호흡이라고 합니다.
다양한 병리를 진단할 수 있는 연구 방법은 다음과 같습니다.
- 스피로그래피.
- 신체 혈량측정.
- 호기 공기의 가스 구성 연구.
중요한! 호흡 기능 분석의 처음 4가지 방법을 사용하면 강제 폐활량, 폐활량, 분당 폐량, 잔류 폐량, 총 폐량은 물론 최대 및 최대 호기 유량을 자세히 연구할 수 있습니다. 폐에서 나오는 공기의 가스 구성은 특수 의료용 가스 분석기를 사용하여 연구됩니다.
이와 관련하여 독자는 FVD 검사와 폐활량 측정이 동일하다는 잘못된 인상을 받을 수 있습니다. 호흡 기능에 대한 연구는 폐활량 측정을 포함하는 전체 테스트 세트라는 점을 다시 한 번 강조하겠습니다.
징후 및 금기 사항
상부 호흡 기능에 대한 포괄적인 테스트에 대한 적응증이 있습니다.
여기에는 다음이 포함됩니다.
- 기관지염, 폐렴, 폐 조직의 폐기종, 비특이적 폐 질환, 기관염, 다양한 형태의 비염, 후두 기관염, 횡경막 손상을 나타내는 어린이를 포함한 환자.
- COPD(만성폐쇄성폐질환)의 진단 및 조절.
- 위험한 생산 지역(먼지, 광택제, 페인트, 비료, 광산, 방사선)과 관련된 환자 검사.
- 만성기침, 호흡곤란.
- 수술을 준비하기 위한 상부 호흡 검사 및 폐의 침습적(생체 조직 채취) 검사.
- 만성 흡연자와 알레르기가 있는 사람을 검사합니다.
- 프로 운동선수는 증가된 신체 활동 하에서 폐의 최대 능력을 결정합니다.
동시에 특정 상황으로 인해 설문 조사를 수행할 수 없는 제한 사항이 있습니다.
- 대동맥의 동맥류(벽의 돌출)입니다.
- 폐나 기관지에서 출혈이 발생합니다.
- 모든 형태의 결핵.
- 기흉은 다량의 공기나 가스가 흉막 부위에 축적되는 경우입니다.
- 복강 또는 흉강 수술 후 1개월 이내.
- 뇌졸중이나 심근경색 이후에는 3개월이 지나야 연구가 가능하다.
- 지적 지체 또는 정신 장애.
전문가의 비디오:
연구는 어떻게 진행되나요?
FVD 연구 절차가 완전히 고통스럽지 않은 과정이라는 사실에도 불구하고 가장 객관적인 데이터를 얻으려면 준비에 신중하게 접근해야 합니다.
- FVD는 공복에 실시하며 항상 아침에 실시합니다.
- 흡연자는 검사 4시간 전부터 담배를 금해야 합니다.
- 연구 당일 신체 활동은 금지됩니다.
- 천식 환자의 경우 흡입 절차를 피하십시오.
- 피험자는 기관지를 확장시키는 약물을 복용해서는 안됩니다.
- 커피나 기타 카페인이 함유된 토닉 음료를 마시지 마십시오.
- 검사 전에 호흡을 제한하는 옷과 그 요소(셔츠, 넥타이, 바지 벨트)를 느슨하게 하십시오.
- 또한 필요한 경우 의사의 추가 권장 사항을 따르십시오.
연구 알고리즘:

기관지의 개통성을 손상시키는 방해가 의심되는 경우 테스트를 통한 FVD가 수행됩니다.
이 테스트는 무엇이며 어떻게 진행되나요?
클래식 버전의 폐활량 측정법은 폐와 기관지의 기능 상태에 대한 최대이지만 불완전한 그림을 제공합니다. 따라서 천식의 경우 벤톨린(Ventolin), 베로두알(Berodual), 살부타몰(Salbutamol) 등 기관지 확장제를 사용하지 않고 기계를 이용한 호흡검사로는 숨은 기관지경련을 발견할 수 없어 간과하게 된다.
예비 결과는 즉시 준비되지만 여전히 의사가 해독하고 해석해야 합니다. 이는 질병이 발견된 경우 질병 치료를 위한 전략과 전술을 결정하는 데 필요합니다.
FVD 결과의 해석
모든 테스트 활동이 완료된 후 결과는 스피로그래프의 메모리에 입력되며, 그곳에서 소프트웨어를 사용하여 처리되고 그래픽 도면(스피로그램)이 구성됩니다.
컴퓨터에 의해 생성된 예비 출력은 다음과 같이 표현됩니다.
- 표준;
- 폐쇄성 장애;
- 제한적 장애;
- 혼합 환기 장애.
의사는 외부 호흡 기능 지표, 규제 요구 사항 준수 여부를 판독한 후 환자의 건강 상태에 대한 최종 판결을 내립니다.
연구된 지표, 호흡 기능의 표준 및 가능한 편차는 일반 표에 나와 있습니다.
| 지표 | 기준(%) | 조건부 비율(%) | 경미한 장애(%) | 평균 손상 정도(%) | 심각한 손상 정도(%) |
|---|---|---|---|---|---|
| FVC – 폐의 강제 폐활량 | ≥ 80 | 79.5-112.5(m) | 60-80 | 50-60 | < 50 |
| FEV1/FVC – 수정됨. 티프노 지수 (절대값으로 표현) |
≥ 70 | 84.2-109.6(m) | 55-70 | 40-55 | < 40 |
| FEV1 – 처음 1초 동안 강제 호기량 | ≥ 80 | 80.0-112.2(m) | 60-80 | 50-60 | < 50 |
| MOS25 - FVC의 25%에서 최대 체적 유량 | > 80 | 70-80 | 60-70 | 40-60 | < 40 |
| MOS50 – FVC의 50%에서 최대 체적 유량 | > 80 | 70-80 | 60-70 | 40-60 | < 40 |
| SOS25-75 – FVC의 25-75% 수준에서 호기 흐름의 평균 체적 속도 | > 80 | 70-80 | 60-70 | 40-60 | < 40 |
| MOS75 – FVC의 75%에서 최대 체적 유량 | > 80 | 70-80 | 60-70 | 40-60 | < 40 |
중요한! FVD 결과를 해독하고 해석할 때 의사는 진단적으로 유용한 FVC, FEV1 및 Tiffno 지수이기 때문에 처음 세 가지 지표에 특별한 주의를 기울입니다. 이들 사이의 관계에 따라 환기 장애의 유형이 결정됩니다.
 이 발음하기 어려운 이름은 강제(최대 힘) 호기 동안 최대 체적 유량을 측정할 수 있는 검사 방법에 붙여졌습니다.
이 발음하기 어려운 이름은 강제(최대 힘) 호기 동안 최대 체적 유량을 측정할 수 있는 검사 방법에 붙여졌습니다.
간단히 말해서, 이 방법을 사용하면 환자가 숨을 내쉬는 속도를 파악하여 최대한의 노력을 기울일 수 있습니다. 이것은 호흡 통로가 좁아졌는지 확인합니다.
천식과 COPD로 고통받는 환자는 특히 최대 유량 측정이 필요합니다. 수행된 치료 조치의 결과에 대한 객관적인 데이터를 얻을 수 있는 사람은 바로 그녀입니다.
피크 유량계는 눈금이 표시된 튜브로 구성된 매우 간단한 장치입니다. 개인이 사용하는데 어떻게 유용합니까? 환자는 독립적으로 측정을 수행하고 복용하는 약물의 복용량을 처방할 수 있습니다.
장치는 매우 간단하여 어른은 물론 어린이도 사용할 수 있습니다. 그건 그렇고, 이러한 간단한 장치의 일부 모델은 특히 어린이를 위해 생산됩니다.
피크 유량 측정은 어떻게 수행됩니까?
테스트 알고리즘은 매우 간단합니다.

데이터를 해석하는 방법은 무엇입니까?
폐호흡 기능을 연구하는 방법 중 하나인 최대 유량 측정법은 최대 호기 유량(PEF)을 측정한다는 점을 독자에게 상기시켜 드리겠습니다. 올바른 해석을 위해서는 녹색, 노란색, 빨간색의 세 가지 신호 영역을 직접 식별해야 합니다. 최대 개인 결과를 기준으로 계산된 특정 범위의 PSV를 특성화합니다.
실제 기술을 사용하는 조건부 환자의 예를 들어 보겠습니다.
- 그린존. 이 범위에는 천식의 완화(약화)를 나타내는 값이 있습니다. PEF가 80% 이상이면 이 상태의 특징이 됩니다. 예를 들어 환자의 개인 기록인 PSV는 500l/min입니다. 계산해 봅시다: 500 * 0.8 = 400 l/min. 우리는 녹색 영역의 아래쪽 경계를 얻습니다.
- 옐로우 존. 이는 기관지 천식의 활성 과정의 시작을 특징으로 합니다. 여기서 하한은 PSV의 60%입니다. 계산 방법은 동일합니다: 500 * 0.6 = 300 l/min.
- 레드존. 이 부문의 지표는 천식의 활성 악화를 나타냅니다. 상상할 수 있듯이 PSV의 60% 미만의 모든 값은 이 위험 영역에 속합니다. "가상" 예에서 이는 300l/min 미만입니다.

혈액 내 산소량을 연구하는 비침습적(침투 없음) 방법을 맥박 산소 측정법이라고 합니다. 이는 혈액 내 헤모글로빈 양에 대한 컴퓨터 분광광도계 평가를 기반으로 합니다.
의료 행위에 사용되는 맥박 산소 측정에는 두 가지 유형이 있습니다.

측정 정확도 측면에서는 두 방법 모두 동일하지만 실용적인 관점에서는 두 번째 방법이 가장 편리합니다.
맥박 산소측정의 적용 분야:
- 혈관외과 및 성형외과. 이 방법은 산소를 포화시키고 환자의 맥박을 조절하는 데 사용됩니다.
- 마취 및 소생술. 청색증(점막과 피부가 푸른색으로 변색되는 현상)을 고치기 위해 환자를 움직일 때 사용합니다.
- 산과학. 태아 산소 측정을 기록합니다.
- 요법.이 방법은 치료 효과를 확인하고 무호흡증(호흡을 멈출 위험이 있는 호흡 병리) 및 호흡 부전을 해결하는 데 매우 중요합니다.
- 소아과. 아픈 아이의 상태를 모니터링하기 위한 비침습적 도구로 사용됩니다.
맥박 산소 측정법은 다음 질병에 처방됩니다.
- COPD(만성 폐쇄성 폐질환)의 복잡한 과정;
- 비만;
- 폐성심(심장의 오른쪽 방의 확대 및 확장);
- 대사 증후군(대사 장애의 복합체);
- 고혈압;
- 갑상선 기능 저하증(내분비계 질환).
표시:
- 산소 요법 중;
- 불충분한 호흡 활동;
- 저산소증이 의심되는 경우;
- 장기간 마취 후;
- 만성 저산소혈증;
- 수술 후 재활 기간 동안;
- 무호흡증 또는 그에 대한 전제 조건.
중요한! 일반적으로 헤모글로빈으로 포화된 혈액의 경우 그 수치는 거의 98%입니다. 90%에 가까운 수준에서는 저산소증이 명시됩니다. 포화율은 약 95% 여야 합니다.
혈액가스 연구
인간의 경우 혈액의 가스 구성은 일반적으로 안정적입니다. 신체의 병리 현상은 이 지표가 한 방향 또는 다른 방향으로 이동하여 표시됩니다.
표시:
- 환자의 폐 병리 확인, 산-염기 불균형 징후의 존재. 이는 COPD, 당뇨병, 만성 신부전과 같은 질병에서 나타납니다.
- 메트헤모글로빈혈증으로 일산화탄소 중독 후 환자의 건강 상태를 모니터링합니다. 이는 혈액 내 메트헤모글로빈 수치가 증가한 징후입니다.
- 강제 환기에 연결된 환자의 상태를 모니터링합니다.
- 마취과 의사는 특히 폐 수술을 수행하기 전에 데이터가 필요합니다.
- 산-염기 장애의 결정.
- 혈액의 생화학적 조성 평가.
혈액가스 성분의 변화에 대한 신체의 반응
산-염기 균형 pH:
- 7.5 미만 – 신체가 이산화탄소로 과포화되어 있습니다.
- 7.5 이상 – 체내 알칼리 양이 초과되었습니다.
산소 분압 수준 PO 2: 정상 값 아래로 떨어짐< 80 мм рт. ст. – у пациента наблюдается развитие гипоксии (удушье), углекислотный дисбаланс.
이산화탄소 PCO2의 부분압 수준:
- 결과는 정상 수치인 35mmHg보다 낮습니다. 미술. – 신체가 이산화탄소 부족을 느끼고, 과호흡이 완전히 수행되지 않습니다.
- 표시기는 정상 45mmHg 이상입니다. 미술. – 체내에 이산화탄소가 과잉되고, 심박수가 감소하며, 환자는 설명할 수 없는 불안감에 사로잡힙니다.
중탄산염 HCO3 수준:
- 보통 이하의< 24 ммоль/л – наблюдается обезвоживание, характеризующее заболевание почек.
- 정상 값 > 26mmol/l를 초과하는 지표 - 이는 과도한 환기(과호흡), 대사성 알칼리증 및 스테로이드 물질의 과다 복용에서 관찰됩니다.

의학에서 호흡 기능에 대한 연구는 인간 호흡 기관의 상태에 대한 심오하고 일반화된 데이터를 얻기 위한 가장 중요한 도구이며, 인간의 삶과 활동의 전체 과정에 미치는 영향은 과대평가할 수 없습니다.
기관지 과민반응의 검출
정상적인 호흡 기능 지표가 있는 경우유지된 신체 활동을 통한 FVD(6분 달리기 프로토콜) – 폐쇄 징후의 출현(IT 감소, FEV1 15% 이상)은 신체 활동, 즉 기관지 과민반응에 반응하여 병리학적 기관지 경련이 발생했음을 나타냅니다.
약물 검사를 통한 FVD(기관지 확장제 흡입)유지된 초기 호흡 기능에 장애 징후가 있는 경우그 가역성을 공개합니다. FEV1과 IT의 12% 이상 증가는 기관지 폐쇄(기관지 경련)의 가역성을 나타냅니다.
피크 유량
방법론.환자의 최대 유량 측정기 장치 5세 이상숨을 내쉰다. 장치 눈금의 슬라이더 판독값에 따라 PEF가 측정됩니다. 최대 호기 유량(l/min)은 FEV1과 상관 관계가 있습니다. PEF 지표는 최대 11세까지의 표준 데이터와 비교되며 지표는 성별과 신장에만 의존하고 15세부터는 성별, 신장 및 연령에 따라 달라집니다.
어린이와 청소년의 PSV(l/min) 평균 적정값
|
높이(cm) |
PSV(l/분) |
높이(cm) |
PSV(l/분) |
PEF 지표가 평균 규범 값의 60-80%인 "노란색 복도"에 속하는 경우 공격이 발생할 가능성이 있음을 나타냅니다.
PEF 지표가 평균 규범 값의 60% 미만인 "빨간색 복도"에 속하는 경우 이는 천식 발작을 나타내며 긴급 치료 조치가 필요합니다.
검사한 수치는 정상입니다평균 기준의 80% 이상이어야 합니다.("녹색 복도")
아침과 저녁 PSV 데이터 비교 - 가변성그들 사이에 20%를 초과해서는 안 된다.(그림 -1), 하루 변동폭이 20% 이상인 경우 일일 변동입니다(그림 -2).
아침 지표와 전날 저녁 지표의 차이를 알아보세요. 20% 이상이면 기관지 과민반응의 징후입니다(“ 아침 실패" - 쌀. -삼).
최대 유량 측정은 치료의 적절성을 모니터링하는 데 사용됩니다. 아침과 저녁 값 사이의 변동이 증가하면 치료를 늘려야 합니다.
가래검사
Charcot-Leyden 결정(호산구 분해 산물) – 기관지 천식용.
Kurshman 나선(기관지의 점액 캐스트) - 기관지 천식에 사용됩니다.
탄력 섬유 - 결핵, 폐 조직 부패(농양)용.
디트리히 플러그 - 화농성 플러그 - 기관지 확장증용.
코흐 렌즈 - 쌀알 형태의 형성 - 폐 조직 붕괴로 인한 결핵.
종양 세포.
Hemosiderophages는 폐혈철증, 폐경색의 징후입니다.
일일 수량
일반적인 외관(장액성, 점액성, 화농성, 혈성)
현미경 검사:
가래의 세균학적 검사– 결핵 병원체, 병원성 식물상 배양
흉막액 검사
비중 1015 이상
단백질 함량 - 2~3% 이상
양성 Rivalta 반응(보통 음성)
호중구는 급성 세균성 염증의 징후입니다
림프구 – 결핵용
단백질 30g/l 미만
1 입방 밀리미터당 백혈구 수는 2000개 미만이며, 단핵 세포가 우세합니다.
염증성 성격 - 삼출하다
비염증성 - 삼투하다
심장학
정점 투영 마음신생아의 경우 4번째 늑간 공간에 위치하며,
1.5세부터 - 5번째 늑간 공간.
에이펙스 임펄스 -엘 현지화:
IV에서는 최대 1.5년, 그 다음에는 V 늑간 공간(수평선)에서.
2년까지의 수직선은 왼쪽 SCL에서 바깥쪽으로 1-2cm 떨어져 있습니다.
2~7세 - SCL에서 바깥쪽으로 1cm.
7~12세 - 왼쪽 SCL에 따르면.
12세 이상 – SCL에서 안쪽으로 0.5cm.
정사각형- 1 x 1, 더 큰 어린이용 2 x 2 cm.
OST의 왼쪽 테두리정점 충동과 일치합니다.
상대적인 심장 둔함과 심장의 가로 크기의 경계
|
어린이의 나이 |
||||
|
12세 이상 |
||||
|
오른쪽 흉골주위선 |
오른쪽 흉골주위선에서 안쪽 |
오른쪽 흉골주위선과 오른쪽 흉골선 사이의 중간 |
오른쪽 흉골선과 오른쪽 흉골선 사이의 중앙, 후자에 가까운 곳, 이하 오른쪽 흉골선이라 함 |
|
|
II 늑간 공간 | ||||
|
왼쪽 쇄골 중앙선에서 바깥쪽으로 2cm |
왼쪽 쇄골 중앙선에서 바깥쪽으로 1cm |
왼쪽 쇄골 중앙선을 따라 |
왼쪽 쇄골 중앙선에서 안쪽으로 0.5-1cm |
|
|
가로 사이즈 | ||||
톤의 소리는 연령에 따라 다릅니다.
생후 첫 2~3일 동안 첫 번째 청진 지점(첨부) II>I, 그 다음에는 I=II, 정상 생활의 2~3개월나톤 >II.
마음을 바탕으로(청진의 두 번째 및 세 번째 지점) 1년차에 I>II, 그 다음에는 I=II, 3세부터II> 나.
괜찮은 2세부터 12세까지II폐동맥 위(왼쪽)의 톤이 더 강함II대동맥 위의 톤(오른쪽)(“증가IIl/a" 이상의 톤). 12세부터 이 음색의 소리를 비교합니다.
일반적으로 세 번째 톤(두 번째 톤 이후 조용하고 짧음)이 있을 수 있습니다. 청진의 다섯 번째 지점에서는 누운 상태에서만 서 있는 자세에서 사라집니다.
일반 톤은 울림이 있습니다.– I 및 II 톤의 비율은 연령 특성에 해당합니다(I>II 톤 상단의 수명 2~3개월).
평소에는 톤이 맑아요~분할되지 않은 컴팩트. 그러나 아마도 생리적 분열II음색– 대동맥 판막과 폐동맥 판막의 비동시 폐쇄 또는 심실의 비동시 수축으로 인해(나중에 더 많은 혈액량으로 인해 좌심실 확장기 발생). 들었다 마음에 기초를 두고, 영원하지 않습니다.
맥박리듬 - 2~11세의 건강한 어린이는 호흡 부정맥(숨을 들이쉬면 심박수가 증가하고, 숨을 내쉬면 감소하며, 숨을 참으면 맥박이 리듬이 됩니다).
무기 소음
폐동맥 너머로 들림(정점에서는 덜 자주) 혈액 점도가 변할 때 혈액 난류로 인해 높은 충격 방출:
VSD, 빈혈, 발열, 갑상선 중독증, 만성 편도선염.
기능의– 다른 장기 및 시스템에 질병이 있지만 심장은 건강합니다.
생리적= 무고함 = 우발적 = 심장 형성 잡음 – 건강한 어린이의 경우 AFO CVS로 인해 발생 – 미취학 아동 및 미취학 아동의 경우 더 자주 들림 폐동맥 위(최대 7년, 심장내막 내부 표면의 소주망 발달 증가, 혈류 속도 증가, 혈관 직경 넓어짐, 판막 및 화음의 고르지 않은 성장).
|
무기 소음의 징후 |
유기 소음의 징후 |
|
수축기 전용 |
수축기, 확장기, 수축기-이완기일 수 있습니다. 이완기 심잡음의 존재는 즉시 유기적 기원을 나타냅니다. |
|
톤과 관련 없음 |
일반적으로 톤과 관련이 있습니다. |
|
1/3-1/2 수축기 이하 |
장기간 - 수축기의 절반 이상 |
|
l/a 위에는 더 자주, 정점에서는 덜 자주 |
어느 시점에서든 2개 이상의 유기적 기원을 듣습니다. |
|
방출하지 마십시오 |
방사선 조사의 존재는 유기물의 표시입니다 |
|
조용하거나 적당히 큰 소리 |
시끄럽고 무례하다면 - 유기적 기원 |
|
깊은 영감을 받으면 약화되거나 사라집니다. |
심호흡을 해도 변하지 않는다 |
|
부하에 따라 사라지거나 감소함 |
로딩 후에는 변경되거나 증가하지 않습니다. |
|
웨지 자세(누운 자세)에서 더 잘 들리고, 직교 자세로 움직일 때 약해지거나 사라집니다. |
직교 위치로 이동하면 유지되거나 향상됩니다. |
|
FKG에서 - 낮은 진폭, 낮은 빈도 |
FKG - 높은 진폭, 고주파수 및 중간 주파수 |
|
ECG에는 큰 변화가 없습니다. |
ECG - 단면 비대 징후 |
|
Echo-CG는 유기적 심장 손상의 징후를 보이지 않습니다(정상적인 공동 크기 및 심근 두께, 높은 박출률(EF 65% 이상), 변하지 않은 판막, 자유 심낭 공간) |
Echo-CG – 심내막염의 징후, 판막염, 선천성 심장병 또는 후천성 심장병 심장 결함 |
화성 배경의 소음– 경계 소음.
MARS는 전신 혈역학, 심장 크기 또는 수축성의 변화를 동반하지 않는 심장 형성 장애입니다. 이는 추가 화음, 화음 위치의 이상 및 승모판 탈출증입니다.
변하기 쉬운딸깍거리는 소리나 부는 소리, 음악적 톤이 들리지 않습니다. 서 있을 때 더 잘 들을 수 있습니다.
불만 사항도 없고, 혈역학적 장애의 징후도 없으며, 심장 경계도 정상입니다.
낙인 수준 증가(짧고 구부러진 작은 손가락...), 자세 장애, 시각 기관, HMS 발현.
심낭 마찰 문지름
톤이 안맞네요. 청진기로 누를 때, 심호흡을 하면서 숨을 참을 때, 앞으로 구부릴 때 더욱 심해집니다.
처음에는 현지 장소에서 들립니다. 판막 청진 장소와 일치하지 않고 심장 전체 영역으로 퍼집니다.
심장 너머로 방출되지 않습니다(“태어난 곳에서 죽습니다”).
순환부전의 단계(CI)
맥박수, 서맥, 빈맥의 연령 기준(V.K. 타토첸코, 1997)
|
서맥 |
빈맥 |
||||||
|
보통의 |
중요한 |
보통의 |
중요한 |
||||
혈압 평가
정상 혈압– 혈압 분포 곡선의 10-89 백분위수.
하이 노멀(정상의 상한) - 90-94 백분위 수.
동맥성 고혈압– 해당 성별, 연령 및 키에 대한 혈압 분포 곡선의 95번째 백분위수 이상입니다.
동맥 저혈압– 3백분위수 미만.
낮은 정상 혈압(정상의 하한) – 4-10 백분위수.
측정 결과가 10분위수 미만 및 90백분위수 초과 영역에 해당하는 경우 정기적으로 반복 혈압 측정을 통해 어린이를 특별 관찰해야 합니다. 아이의 혈압이 다시 3백분위수 이하 또는 95백분위수 이상인 경우에는 검사가 필요합니다.동맥 저혈압 또는 고혈압의 원인을 파악하기 위해 전문 소아 심장학 클리닉에서.